Imunosni sustav se sastoji od stanična i molekularna komponenata koje se udružuju radi uništavanja antigena. (Vidi također Pregled imunosnog sustava.)
Antigen–predočne stanice
Premda neki antigeni (Ag-i) mogu izravno stimulirati imunosni odgovor, stečeni imunosni odgovori ovisni o T stanicama u pravilu zahtijevaju antigen–predočne stanice (APC-e, prema engl. antigen presenting cells) koje predočuju peptide antigenog podrijetla unutar molekula glavnog kompleksa tkivne podudarnosti (MHC).
Unutarstanični antigeni (npr. virusi) mogu biti prerađeni i predočeni CD8 citotoksičnim T stanicama pomoću bilo kojih stanica s jezgrama jer sve one eksprimiraju MHC molekulu klasa I. Kodiranjem proteina koji utječu na ovaj proces, neki virusi (npr. citomegalovirus) mogu izbjeći eliminaciju.
Izvanstanični antigeni (npr. od mnoge bakterije) moraju biti prerađeni u peptide i složeni unutar MHC molekula klasa II na staničnoj površini profesionalnih antigen–predočnih stanica da bi ih mogle prepoznati CD4 pomoćničke (Th) stanice. Sljedeće stanice konstitutivno eksprimiraju MHC molekulu klasa II i stoga djeluju kao profesionalnih antigen–predočnih stanica:
-
B stanice
-
Monociti
-
Makrofagi
-
Dendritičke stanice
Monociti koji se nalaze u krvotoku su preteče (prekursori) tkivnih makrofaga. Monociti migriraju u tkiva, gdje se kroz otprilike 8 sati razvijaju u makrofage pod utjecajem faktora koji stimulira kolonije makrofaga (M–CSF, prema engl. macrofage colony–stimulating factor), kojeg luče različite vrste stanica (npr. endotelne stanice, fibroblasti). Na mjestima infekcije, aktivirane T stanice luče citokine (npr. interferon gama [IFN–γ]) koji induciraju stvaranje faktora koji inhibira migraciju makrofaga, sprečavajući odlaska makrofaga.
Makrofage aktiviraju IFN-gamma i faktor stimulacije kolonija granulocitnih makrofaga (GM-CSF). Aktivirani makrofagi uništavaju unutarstanične organizme i izlučuju IL–1 te faktor tumorske nekroze-α (TNF–α, prema engl. tumor necrosis factor α). Ovi citokini pojačavaju izlučivanje IFN–gama i GM–CSF–a te povećavaju ekspresiju adhezijskih molekula na endotelnim stanicama, olakšavajući time prodor leukocita i razaranje patogena. Na temelju različitih profila genske ekspresije, podtipovi makrofaga (npr. M1, M2) su identificirani.
Podvrste makrofaga
|
Karakteristike
|
M1
|
M2
|
|
IFN = interferon; IL = interleukin; Th1 stanice = pomoćničke T stanice tip 1; Th2 stanice = pomoćničke T stanice tip 2; TNF = tumorski faktor nekroze.
|
|
Sredstvo za aktivaciju
|
Stimulacija Toll-like receptora
IFN-gama (citokin koji proizvodi Th1 stanice)
|
IL-4 i IL-13 (citokini koji proizvodi Th2 stanice)
|
|
Proizvedeni citokini
|
Proupalni citokini (npr. TNF-alfa)
|
Imunosupresivni citokini (npr. IL-10)
|
|
Ostale funkcije
|
Promicanje Th1 odgovora
Snažno mikrobicidno
|
Promicanje remodeliranje tkiva
|
Dendritične stanice se nalaze u koži (kao Langerhansove stanice), limfnim čvorovima i tkivima u cijelom tijelu. Dendritične stanice u koži se ponašaju kao stražarske antigen–predočne stanice, koje nakon prihvaćanja antigen putuju do lokalnih limfnih čvorova gdje mogu aktivirati T stanice. Folikularne dendritične stanice različitog su podrijetla, ne eksprimiraju MHC molekulu klasa II i zato ne predočavaju antigene Th stanicama. Ne fagocitiraju; posjeduju receptore za regiju kristalizirajućeg fragmenta (Fc) IgG-a i za komplement, što im omogućuje vezivanje za imune komplekse koje predočavaju B stanicama u germinativnim centrima sekundarnih limfatičnih organa.
Limfociti
Dvije glavne vrste limfocita su
Morfološki se ne razlikuju, no imaju različite imunosne funkcije. Mogu se razlikovati po površinskim receptorima koji su specifični za antigen i molekulama koji se zovu klasteri diferencijacije (prema engl. CD) prema čijem se prisustvu ili odsustvu definira određena podvrsta stanica. Dosad je identificirano >300 CD molekula (CD antigeni su detaljno opisani u CD indeksu na http://mpr.nci.nih.gov/prow). Svaki limfocit prepoznaje specifični antigen preko površinskih receptora.
B stanice
Otprilike 5 do 15% limfocita u krvi su B stanice; također su prisutni u koštanoj srži, slezeni, limfnim čvorovima te limfatičnom tkivu sluznica
B stanice mogu predočiti antigen T stanicama i oslobađaju citokine, ali njihova primarna funkcija je razviti u plazma stanice, koje proizvode i izlučuju protutijela.
Pacijenti s imunodeficijencijom B stanica (npr. X-vezana agamaglobulinemija) su posebno osjetljivi na rekurentne bakterijske infekcije.
Nakon nasumičnog preuređenja gena koji kodiraju imunoglobulin, B stanice imaju potencijal prepoznavanja gotovo neograničenog broja jedinstvenih antigena. Gensko preuređenje se događa prema programiranim koracima u koštanoj srži tijekom razvoja B stanica. Proces započinje s usmjerenom matičnom stanicom, nastavlja se kroz pro–B i pre–B stanične faze i rezultira stvaranjem nezrele B stanice. U ovom trenutku, sve stanice koje su u interakciji s vlastitom antigenom (autoimuna stanica) se ukloni iz populacije nezrelih B stanica putem inaktivacije ili apoptoze (imuna tolerancija). Nezrele B stanice koje nisu uklonjene (tj. one koje prepoznaju strani antigen) mogu nastaviti svoj razvoj prema zrelim naivnim B stanicama, napustiti koštanu srž i ući u periferne limfatične organe, gdje mogu naići na antigene.
Njihov odgovor na antigen ima 2 faze:
-
Primarni imunosni odgovor: kada zrele naivne B stanice prvi put dođu u kontakt s antigenom, postaju limfoblasti, podvrgavaju se klonskoj proliferaciji te diferencijaciji u memorijske stanice, koje mogu odgovoriti na isti antigen u budućnosti ili pak postaju zrele plazma stanice koje proizvode protutijela. Nakon prvog izlaganja, ima latentni period od nekoliko dana prije nego što se protutijelo proizvodi. Zatim, samo se proizvodi IgM. Nadalje, pomoću T stanica, B stanice mogu dalje preurediti njihove Ig gene i preusmjeriti proizvodnju prema IgG, IgA ili IgE. Dakle, kod prvog izlaganja, odgovor je spor i osigurava ograničenu zaštitnu imunost.
-
Sekundarni (anamnestički ili pojačivački) imunosni odgovor: kada se memorijske B i Th stanice ponovno izlože antigenu, memorijske B stanice se brzo proliferiraju, diferenciraju u zrele plazma stanice i odmah proizvode velike količine protutijela (uglavnom IgG zbog izotipskog prekapčanja posredovanog T stanicama). Protutijela su otpuštana u krv i ostala tkiva, gdje se može reagirati s antigenom. Dakle, nakon ponovnog izlaganja, imunosni odgovor je brži i učinkovitiji.
T stanice
T stanice nastaju od matičnih stanica u koštanoj srži i putuju u timus, gdje prolaze strogu selekciju. Postoje 3 glavne vrste T stanica:
Tijekom selekcije, T stanice koje reagiraju s vlastitim antigenima koji su predočene na vlastitim MHC molekulama ili sa samim MHC molekulama (bez obzira na antigen koji je predočen), eliminiraju se apoptozom. Samo T stanice koje mogu prepoznati strane antigene koji su vezani u komplekse s vlastitim MHC molekulama preživljavaju; napuštaju timus te odlaze u perifernu krv i limfatična tkiva.
Većina zrelih T-stanice eksprimiraju ili CD4 ili CD8 i ima antigen-vezujuće površinske receptore nalik na imunoglobulinu koji se zovu T stanični receptor (TCR). Postoje dvije vrste TCR-a:
Geni koji kodiraju TCR, kao Ig geni, preuređuje se što dovodi do definirane specifičnosti i afiniteta za antigene. Većina T-stanice (one s alfa-beta TCR-ima) prepoznaju peptide antigenog podrijetla predočene na MHC molekulu antigen-predočne stanice. Gama-delta T-stanice prepoznaju antigen proteina izravno ili prepoznaju antigen lipida predočen na MHC-sličnom molekulu koja se zove CD1. Što se tiče B stanica, količina specifičnosti T-stanica je gotovo neograničena.
Da bi se alfa-beta T-stanice aktivirale, TCR se mora reagirati s antigenom-MHC (vidi sliku Dvo-signalni model za aktivaciju T-stanica). Kostimulirajuće pomoćne molekule također moraju reagirati (npr. CD28 na T stanicama reagiraju s CD80 i CD86 na antigen-predočnim stanicama); inače, T-stanica postaje anergična ili umire apoptozom. Neke dodatne molekule (npr. CTLA-4 na T stanici, koji također reagira s CD80 i CD86 na antigen-predočnoj stanici, PD-1 na T stanici, koji reagira s PD-L1 na antigen-predočnoj stanici) inhibiraju prethodno aktivirane T stanice i time ublaže imunološki odgovor. Molekule kao što su CTLA-4 i PD-1 te njihovi ligandi, nazivaju se molekule kontrolne točke jer signaliziraju da T stanicu treba spriječiti da nastavi svoju aktivnost. Stanice raka koje eksprimiraju molekule kontrolne točke mogu tako biti zaštićene od imunosnog sustava ograničavanjem aktivnosti tumor-specifičnih T stanica.
Monoklonska protutijela koja ciljaju molekule kontrolne točke na T stanicama ili na tumorskim stanicama (takozvani inhibitori kontrolne točke, vidi tablicu Neki imunoterapijski agensi u kliničkoj praksi) se upotrebljavaju za sprječavanje regulacije antitumorskih odgovora i za učinkovito liječenje nekih dosad otpornih karcinoma. Međutim, budući da su molekule kontrolne točke također uključene u druge tipove imunosnog odgovora, inhibitori kontrolne točke mogu uzrokovati ozbiljne imunološke povezane upalne i autoimune reakcije (i sistemske i specifične za organe).
Polimorfizmi u genu CTLA-4 je povezan s određenim autoimunim poremećajima, uključujući Gravesova bolest i dijabetes melitus tip I.
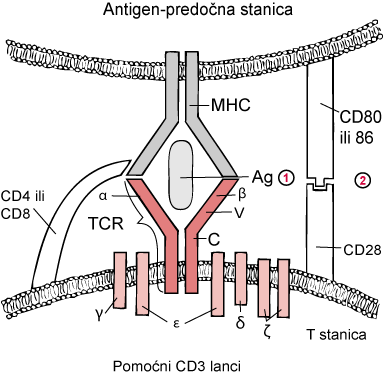
Dvo-signalni model za aktivaciju T stanica
|
α) i β lanci T staničnih receptora (TCR) povezuju antigen (Ag)-glavni kompleks tkivne podudarnosti (MHC) na antigen-predočnoj stanici (APC), te CD4 ili CD8 reagiraju s MHC-om. Obje akcije stimuliraju T stanice (prvi signal) preko pomoćnim CD3 lancima. Međutim, bez drugog (koaktivacijskog) signala, T stanica je anergična ili tolerantna.
TCR je strukturno homologan B staničnim receptoru; α i β (ili γ i δ) lanci imaju konstantna (C) i varijabilna (V) područja. (1) = 1. signal; (2) = 2. signal.
|
Pomoćničke T (Th) stanice su obično CD4, no mogu biti i CD8. Oni se razlikuju od Th0 stanica na jedan od sljedećih načina:
-
Th1 stanice: općenito, Th1 stanice promiču imunitet posredovan stanicama preko citotoksičnih T-stanica i makrofaga i stoga su posebno uključene u obranu od intracelularnih patogena (npr. virusi). Oni također mogu promicati proizvodnju nekih razreda protutijela.
-
Th2 stanice su posebno sposobne u promicanju proizvodnja protutijela pomoću B stanica (humoralni imunitet) i stoga su posebno uključene u usmjeravanje odgovora usmjereni na izvanstanične patogene (npr. bakterije, parazite).
-
Th17 stanice: Th17 stanica promiču upalu tkiva.
Svaka vrsta stanica izlučuje nekoliko citokina (vidi tablicu Funkcije T stanica). Različiti obrasci proizvodnja citokina identificiraju druge funkcionalne fenotipove Th stanica. Ovisno o stimulirajućem patogenu, Th1 i Th2 stanice mogu, do određene mjere, regulirati aktivnost jednog drugog, što dovodi do dominacije Th1 ili Th2 odgovora.
Funkcije T stanica
|
Vrsta
|
Proizvedene tvari
|
Primarna funkcija
|
|
FasL = Fas ligand; IFN = interferon; IL = interleukin; NK = prirodnoubilačka stanica; Tc= citotoksična T stanica; TGF = transformirajući faktor rasta; Th= pomoćnička T stanica.
|
|
Th1
|
IFN-gama
IL-2
limfotoksin
|
Omogućavanje odgovore makrofaga i citotoksičnih T-stanica
|
|
Th2
|
IL-4
IL-5
IL-6
IL-10
IL-13
|
Stimuliranje proizvodnja protutijela pomoću B stanica
|
|
Th17
|
IL-17
IL-21
IL-22
|
Promicanje upalnih odgovora
|
|
Regulatorna
|
TGF-beta
IL-10
IL-35
|
Umanjenje imunosnih odgovora
|
|
Tc
|
Perforin
Grenzimi
FasL
Citokini
|
Ubijanje zaraženih stanica
|
|
Aktivirane NKT stanice
|
IL-4
IFN-gama
|
Može pomoći u regulaciji imunosnih odgovora
|
Razlika između različitih Th stanica je od kliničkog značaja. Primjerice, Th1 odgovor dominira u tuberkuloidnoj gubi, a Th2 odgovor dominira u lepromatoznoj gubi. Th1 odgovor je karakterističan za određene autoimune poremećaje (npr. dijabetes melitus tip 1, multipla skleroza) i Th2 odgovor promiče proizvodnju IgE i razvoj alergijskih poremećaja, kao i pomaže B stanicama da proizvode autoprotutijela u nekim autoimunim poremećajima (npr. Gravesova bolest, mijastenija gravis). Th17 stanice, preko svoje uloge u upali, može također doprinijeti autoimunim poremećajima kao što su psorijaza i reumatoidni artritis. Pacijenti s imunodeficijencijama karakterizirane defektne Th17 stanice (npr. hiper-IgE [Job] sindrom) su posebno osjetljivi na infekcije Candida albicans i Staphylococcus aureus.
Regulatorne (supresorske) T stanice posreduje suprimiranje imunosnog odgovora i obično eksprimiraju transkripcijski faktor Foxp3. Proces uključuje funkcionalne podvrste CD4 ili CD8 T stanica koje ili luče citokine s imunosupresivnim svojstvima ili suprimiraju imunosni odgovor slabo definiranim mehanizmima koji zahtijevaju interstanični kontakt. Pacijenti s funkcionalnim mutacijama u Foxp3 razvijaju autoimuni poremećaj IPEX sindrom (imunodisregulacija, poliendokrinopatija, enteropatija, X-vezani sindrom).
Citotoksične T (Tc) stanice obično su CD8 ali mogu biti i CD4; one su neophodne za eliminaciju unutarstaničnih patogena, posebice virusa. Tc stanice imaju ulogu u odbacivanju transplantiranog organa.
Razvoj Tc stanica uključuje 3 faze:
-
prekursorska stanica koja se može, kada se prikladno stimulira, diferencirati u Tc stanicu.
-
efektorska stanica koja se diferencirala i može uništiti svoje odgovarajuće ciljeve
-
memorijska stanica koja miruje (ne treba daljnju stimulaciju), ali je spremna postati efektorskom kada dođe do ponovne stimulacije izvornom kombinacijom antigen–MHC.
Potpuno aktivirane Tc stanice, kao prirodnoubilačke stanice, mogu uništiti zaraženu ciljnu stanicu inducirajući apoptozu.
Tc stanice mogu lučiti citokine i, kao Th stanice, su podijeljene u tipove Tc1 i Tc2 na temelju njihovih obrazaca proizvodnja citokina.
Tc stanice mogu biti
-
singeneične: stvorene kao odgovor na vlastite (autologne) stanice modificirane virusnom infekcijom ili nekim drugim stranim proteinima.
-
alogeneične: stvorene kao odgovor na stanice koje eksprimiraju strane MHC produkte (npr. kod transplantacije organa kad se donorske MHC molekule razlikuju od onih u primatelja transplantata).
Neke Tc stanice mogu izravno prepoznati strane MHC (izravni put); druge mogu prepoznati fragmente stranih MHC predočene vlastitim MHC molekulama primatelja transplantata (posredni put).
Prirodnoubilačke T stanice (NKT) su posebnu podskupinu T stanica. Aktivirane NKT stanice izlučuju IL-4 i IFN-gama i mogu pomoći u regulaciji imunosnog odgovora. NKT stanice se razlikuju od NK stanica u fenotipu i određenim funkcijama.
Mastociti
Mastociti se nalaze u tkivima i funkcionalno su slični bazofilima koji cirkuliraju u krvi.
Mukozne mastocitne granule sadrže triptaze te kondroitin sulfat; vezivno tkivne mastocitne granule sadrže triptaza, himaza i heparin. Oslobađajući ovih medijatora, mastociti igraju ključnu ulogu u stvaranju zaštitnih akutnih upalnih odgovora; bazofili i mastociti su izvor reakcije preosjetljivosti tip I povezane s atopičnom alergijom. Degranulacija se može potaknuti križnim vezanjem IgE receptora ili fragmentima anafilatoksina komplementa C3a i C5a.
Prirodnoubilačke (NK) stanice
Tipične prirodnoubilačke (NK) stanice pripadaju kategoriji stanica koje se kolektivno zovu urođene limfne stanice (što uključuje ILC1, ILC2 i ILC3). NK stanice čine 5 do 15% mononuklearnih stanica periferne krvi i imaju okruglu jezgru i granularnu citoplazmu. Induciraju apoptozu u zaraženim ili abnormalnim stanicama brojnim putevima. Poput drugih urođenih limfoidnih stanica, nedostaju antigen-specifični receptori; međutim, nedavni dokazi upućuju na to da neke NK stanice imaju oblik imunološkog pamćenja.
Markeri stanične površine koji najbolje karakteriziraju NK stanice su CD2+, CD3–, CD4–, CD8+, CD16+ (receptor za IgG–Fc) i CD56+.
Tipične NK stanice se smatraju važno za nadzor tumora. NK stanice eksprimiraju aktivirajuće i inhibitorne receptore. Aktivirajući receptori NK stanica mogu prepoznati brojne ligande na ciljnim stanicama (npr. MHC klasa I povezan lanac A [MICA] i lanac B [MICB]); inhibicijski receptori NK stanice prepoznaju MHC molekule klasa I. NK stanice mogu uništiti svoj cilj samo kada nema jakog signala od inhibitornih receptora. Prisutnost MHC molekula klasa I (normalno eksprimirane na stanicama s jezgrama) na stanicama stoga sprječava uništenje stanica; njihovo odsustvo ukazuje na to da je stanica zaražena određenim virusima koji inhibiraju ekspresiju MHC-a ili je izgubila ekspresiju MHC-a jer je rak promijenio stanicu.
NK stanice mogu također lučiti nekoliko citokina (npr. IFN-gama, IL-1, TNF-alfa); oni su glavni izvor IFN-gama. Izlučivanjem IFN-gama, NK stanice mogu utjecati na stečeni imunosni sustav promicanjem diferencijacije pomoćničkih stanica tip 1 (Th1) i inhibiranjem stanica tip 2 (Th2).
Pacijenti s nedostatkom NK stanica (npr. neke vrste teške kombinirane imunodeficijencije) posebno su osjetljivi na infekcije herpesa i humanog papiloma virusa.
Polimorfonuklearni leukociti
Polimorfonuklearni leukociti, također nazvani granulociti iz razloga što njihova citoplazma sadrži granule, uključuju
-
neutrofili
-
eozinofili
-
bazofili
Polimorfonuklearni leukociti su prisutni u cirkulaciji te imaju multilobularne jezgre.
Neutrofili
Neutrofili čine 40 do 70% ukupnog broja cirkulirajućih bijelih krvnih stanica; oni su prva linija obrane protiv infekcija. Zreli neutrofili imaju poluživot od otprilike 2 do 3 dana.
Tijekom akutnog upalnog odgovora (npr. infekcije), neutrofili, privučeni kemotaktičnim faktorima i upozoreni ekspresijom adhezijskih molekula na endotelu krvnih žila, napuštaju cirkulaciju i ulaze u tkiva. Njihova svrha je fagocitoza i probava patogena. Mikroorganizmi bivaju uništeni kada fagocitozom generirani litički enzimi i reaktivne kisikove spojeve (npr. superoksid, hipoklorna kiselina) dovedu do otpuštanja sadržaja granula (npr. defenzina, proteaza, proteina koji povećavaju propusnost bakterijske stijenke, laktoferina i lizozima). DNK i histoni se također otpuštaju, te zajedno sa sadržajem granula, primjerice elastazama, stvaraju vlaknaste strukture koje se nazivaju izvanstanične zamke neutrofila (prema engleskom neutrophil extracellular traps, NETs) u okolnim tkivima čime olakšavaju uništavanje bakterija hvatajući ih te usmjeravaju aktivnost enzima.
Pacijenti s imunodeficijencijama koje utječu na sposobnost fagocita da unište patogene (npr. kronična granulomatozna bolest) posebno su osjetljivi na kronične bakterijske i gljivične infekcije.
Eozinofili
Eozinofili čine do 5% ukupnog broja cirkulirajućih bijelih krvnih stanica.
Njihov cilj su organizmi koji su preveliki da budu prožderani; uništavaju ih lučenjem toksičnih tvari (npr. reaktivni kisikovi spojevi slični onima koje proizvode neutrofili), glavnih bazičnih proteina (toksični za parazite), eozinofilnog kationskog proteina i nekoliko enzima.
Eozinofili su, također, glavni izvor upalnih medijatora (npr. prostaglandina, leukotrijena, faktora aktivacije trombocita, brojnih citokina).
Bazofili
Bazofili čine <5% cirkulirajućih bijelih krvnih stanica te imaju nekoliko zajedničkih odlika kao i mastociti, premda su te dvije stanične linije različitog podrijetla. Obje imaju receptore visokog afiniteta za IgE, nazvane Fc-epsilon RI (FcεRI). Kad se ove stanice susretnu s određenim antigenima, bivalentne IgE molekule vezane za receptor križno se povezuju potičući staničnu degranulaciju s posljedičnim otpuštanjem prethodno stvorenih upalnih medijatora (npr. histamina, faktora aktivacije trombocita) te stvaranje novih sintetiziranih medijatora (npr. leukotrijena, prostaglandina, tromboksana).