Urednica sekcije: prof. prim. dr. sc. Marija Tonkić, dr. med.
Prijevod: dr. sc. Sanda Sardelić, dr. med.
Definicija
Originalna empirijska definicija AIDS-a od strane Centers for Disease Control and Prevention (CDC) glasila je "prisutnost pouzdano dijagnosticirane bolesti koja barem umjereno ukazuje na osnovni poremećaj stanične imunosti". Nakon pronalaženja uzročnog virusa, HIV-a (prije zvanog HTLV-III/LAV) i razvoja osjetljivih i specifičnih testova na infekciju HIV-om, definicija AIDS-a je pretrpjela značajne promjene. Trenutna definicija razvrstava osobe zaražene HIV-om na osnovi kliničkih stanja povezanih s infekcijom HIV-om i broja CD4+ limfocita (Tbl. 173-1 i 173-2, HPIM-16). S praktičnog stajališta, kliničar bi trebao promatrati infekciju HIV-om kao spektar poremećaja u rasponu od primarne infekcije, sa ili bez akutnog HIV sindroma, do asiptomatskog stanja zaraze i uznapredovale bolesti.
Etiologija
AIDS je posljedica infekcije humanim retrovirusima HIV-1 ili HIV-2. HIV-1 je najčešći uzročnik širom svijeta; HIV-2 pokazuje homologiju s HIV-om 1 u oko 40% sekvenci a pronađen je pretežito u zapadnoj Africi. Međutim, infekcija HIV-om 2 je danas opisana u Europi, Južnoj Americi, Kanadi i SAD-u. Ovi se virusi prenose putem spolnog odnosa, krvi, krvnih derivata ili drugih tjelesnih tekućina (kao kod intravenskih narkomana koji dijele igle za intravensku primjenu); tijekom poroda od majke na dijete; ili putem majčinog mlijeka. Nema dokaza da se virus može prenijeti uobičajenim ili obiteljskim kontaktom niti putem kukaca poput komaraca. Postoji konačna, premda mala profesionalna opasnost za zdravstvene radnike i laboratorijsko osoblje koje radi s uzorcima zaraženim HIV-om. Opasnost od prijenosa HIV-a bolesnicima, od strane zaraženog zdravstvenog radnika, invazivnim postupcima iznimno je niska.
Epidemiologija
Procjenjuje se kako je od siječnja 2003., u SAD-u dijagnosticirano 886.575 kumulativnih slučajeva AIDS-a: oko 57% njih je umrlo. Međutim, tijekom posljednjih 10 godina stopa smrtnosti od AIDS-a se znakovito smanjila, u prvom redu zbog povećane primjene moćnih antivirusnih lijekova. Procjenjuje se kako u SAD-u živi između 850.000 i 950.000 ljudi zaraženih HIV-om. Glavne rizične skupine i dalje su muškarci koji održavaju spolne odnose s muškarcima te intravenski narkomani i muškog i ženskog spola (IDU). Međutim, broj slučajeva koji se prenose heteroseksualno se brzo povećava, osobito među ženama (vidi Tbl. 173-5; sl. 173-10 do 173-13, HPIM-16). Budući da se većina slučajeva povezanih s intravenskim drogiranjem javlja u gradskim manjinskim skupinama, teret infekcije HIV-om i AIDS-a sve više, i nesrazmjerno pogađa manjine osobito u gradovima sjeveroistoka i jugoistoka SAD-a. Slučajevi AIDS-a i dalje se pronalaze među osobama koje su u prošlosti primile zaražene krvne derivate, premda je opasnost od zadobivanja nove infekcije ovim putem u SAD-u izuzetno mala. Infekcija HIV-om/AIDS je globalna pandemija, osobito u zemljama u razvoju. Trenutno procijenjeni broj infekcija HIV-om širom svijeta iznosi oko 40 milijuna, od čega su dvije trećine u subsaharskoj Africi; a 50% slučajeva u žena (Sl. 173-9 i Tbl. 173-3, HPIM-16).
Patofiziologija i imunopatogeneza
Glavni znak HIV-om izazvane bolesti je teška imunodeficijencija koja nastaje uslijed progresivnog kvantitativnog i kvalitativnog nedostatka podskupine T limfocita zvanih pomoćničke (helper ili inducer) T stanice. Ova podskupina T stanica fenotipski je definirana iskazivanjem (ekspresijom) CD4 molekule na površini stanica, a koja služi kao primarni stanični receptor za HIV. Za učinkovit ulazak HIV-a 1 u ciljne stanice mora biti prisutan i koreceptor. Dva glavna koreceptora za HIV-1 su CCR5 i CXCR4. Oba ta receptora pripadaju sedmerostrukoj transmembranskoj domeni s G bjelančevinama sparene obitelji receptora. Premda su CD4+ limfociti i pripadnici CD4+ monocitne linije stanica glavne stanične mete HIV-a, praktički svaka stanica koja iskazuje CD4 zajedno s koreceptorima potencijalno može biti zaražena HIV-om.
PRIMARNA INFEKCIJA
Nakon početnog prijenosa, virus inficira CD4+ stanice, vjerojatno limfocite, monocite ili dendritične stanice porijekla koštane srži. Kako tijekom ovog početnog stadija ,tako i kasnije tijekom infekcije, limfatični je sustav glavno sjedište za smještaj i širenje infekcije HIV-om. U početku je arhitektura limfnih čvorova očuvana, no na kraju je potpuno poremećena te se učinkovitost čvorova u zarobljavanju viriona smanjuje, vodeći do uravnoteženosti opterećenja virusom između stanica periferne krvi i stanica u limfnom čvoru.
Većina bolesnika tijekom primarne infekcije prolazi kroz stadij viremije; u nekih je bolesnika ovo povezano s "akutnim retrovirusnim sindromom", bolešću nalik mononukleozi (vidi dalje). Ovaj je stadij važan za rasap (rasijavanje) virusa u limfatične i druge organe te se napokon obuzdava dijelom razvojem za HIV specifičnog imunog odgovora i zarobljavanjem viriona u limfatičnom tkivu.
RAZVOJ KRONIČNE I PERZISTENTNE INFEKCIJE
Unatoč snažnom imunološkom odgovoru koji se razvija nakon primarne infekcije, virus, uz vrlo malo iznimaka ne biva izbačen iz tijela. Umjesto toga, razvija se kronična infekcija koja prosječno traje 10 godina prije nego bolest postane klinički očita. Tijekom tog razdoblja kliničke latencije, broj CD4+ stanica se postupno smanjuje, no nema nikakvih očitih kliničkih znakova ili su oskudni; međutim, aktivno umnožavanje virusa se gotovo uvijek može otkriti mjerljivom viremijom u plazmi te dokazivanjem umnažanja virusa u limfatičnom tkivu. Razina ustaljene viremije (koja se naziva virusnom polaznom točkom), otprilike 1 godinu nakon infekcije ima važan utjecaj na prognozu što se tiče napredovanja bolesti izazvane HIV-om; osobe s niskom virusnom polaznom točkom 6 mjeseci do 1 godine nakon infekcije napredovat će do AIDS-a sporije od onih čiji je polazna točka u to doba vrlo visoka (vidi Sl. 173-17, HPIM-16).
UZNAPREDOVALA BOLEST IZAZVANA HIV-om
U neliječenih bolesnika ili u onih kod kojih liječenje nije uspostavilo nadzor nad umnožavanjem virusa (vidi dalje), nakon određenog vremenskog razdoblja (često nekoliko godina), broj CD4+ T stanica past će ispod kritične razine (oko 200/μL), a bolesnici će postati vrlo podložni oportunističkim bolestima. Međutim, nadzor nad viremijom u plazmi pomoću učinkovitog antiretrovirusnog liječenja je, čak i u osoba s iznimno niskim brojem CD4+ T stanica, produljio preživljenje unatoč činjenici da se u njih broj CD4+ T stanica ne mora znakovito povećati uslijed liječenja.
Imunološki poremećaji u bolesti izazvanoj HIV-om
U bolesnika zaraženih HIV-om je dokazan širok raspon imunoloških poremećaja. Oni obuhvaćaju i kvantitativne i kvalitativne poremećaje funkcije limfocita, monocita/makrofaga i stanica ubojica (NK), kao i razvoj autoimunih pojava.
Imunološki odgovor na infekciju HIV-om
Ubrzo nakon primarne infekcije razvijaju se i humoralni i stanični imunološki odgovori na HIV (vidi sažeto u Tbl. 173-8 i Sl. 173-21 u HPIM-16). Humoralni odgovori uključuju protutijela s aktivnošću vezanja i neutralizacije HIV-a, kao i protutijela koja sudjeluju u o protutijelima ovisnoj staničnoj citotoksičnosti (ADCC). Stanični imunološki odgovori uključuju stvaranje za HIV specifičnih CD4+ i CD8+ limfocita, kao i NK stanica te mononuklearnih stanica koje sudjeluju u ADCC. CD8+ T limfociti mogu također suprimirati umnožavanje HIV-a, na ne-citolitički, ne-MHC ograničeni način. Ovaj je učinak posredovan topljivim faktorima poput CC-kemokina RANTES, MIP-1α i MIP-1β.
Dijagnoza infekcije HIV-om
Laboratorijska dijagnoza infekcije HIV-om ovisi o dokazivanju anti HIV protutijela i/ili o dokazivanju HIV-a ili jedne od njegovih sastavnica.
Standardni test probira na infekciju HIV-om je otkrivanje anti-HIV protutijela pomoću enzimskog imunoeseja (EIA). Ovaj je test jako osjetljiv (>99,5%) i prilično specifičan. Većina komercijalnih EIA kitova može otkriti i HIV-1 i -2. Western blot je test koji se najčešće koristi za potvrđivanje i otkriva protutijela na antigene HIV-a specifične molekularne težine. Protutijela na HIV počinju se pojavljivati unutar 2 tjedna od infekcije, a vremensko razdoblje između početka infekcije i razvoja protutijela koja se mogu otkriti rijetko je >3 mjeseca. HIV p24 antigen se može mjeriti pomoću testa hvatanja (capture analiza) označenog antigena, analize nalik na EIA. Razine p24 antigena u plazmi rastu tijekom prvih nekoliko tjedana nakon infekcije, prije pojavljivanja anti-HIV protutijela. Naputak za primjenu ovih seroloških testova u dijagnostici infekcije HIV-om je prikazan na Sl. 105-1.
HIV se može uzgojiti neposredno iz tkiva, stanica periferne krvi ili plazme, no to se najčešće radi u istraživačke svrhe. Genski materijal HIV-a se može otkriti pomoću PCR-a reverznom transkriptazom (RT-PCR), grananjem DNK (bDNK), ili esejom zasnovanim na sekvenci nukleinskih kiselina (NASBA). Ovi testovi su korisni u bolesnika s pozitivnim ili neodređenim rezultatima EIA ili neodređenim Western blotom ili u bolesnika kod kojih serološko testiranje može biti nepouzdano (poput onih s hipogamaglobulinemijom).
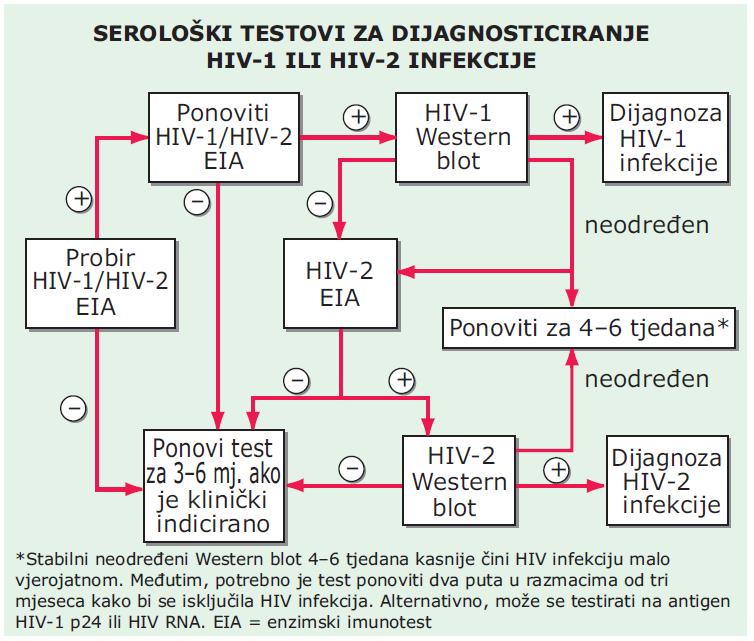
SLIKA 105-1 Algoritam za primjenu seroloških testova pri dijagnostici zaraze s HIV-1 ili HIV-2.
Laboratorijski nadzor bolesnika s HIV infekcijom
Mjerenje broja CD4+ T stanica i razine RNK HIV-a u plazmi su važni dijelovi rutinske procjene i nadzora nad osobama zaraženim HIV-om. Broj CD4+ T stanica je opće prihvaćeni pokazatelj imunološke kompetencije bolesnika s infekcijom HIV-om, a postoji bliska povezanost između broja CD4+ T stanica i kliničkog očitovanja AIDS-a (Sl. 173-26 u HPIM-16). Bolesnici s brojem CD4+ T stanica < 200/μL su u povećanoj opasnosti od razvoja infekcije s Pneumocystis carinii, dok su bolesnici s brojem CD4+ T stanica < 50/μL u povećanoj opasnosti od bolesti izazvane CMV-om i infekcije s Mycobacterium avium intracellulare. Bolesnicima bi broj CD4+ T stanica trebalo određivati u vrijeme postavljanja dijagnoze i svakih 3 do 6 mjeseci nakon toga (u bolesnika kod kojih broj pada mjerenja se mogu obavljati češće). Prema najpraktičnijim naputcima, broj CD4+ T stanica < 350/μL predstavlja indikaciju za započinjanje antiretrovirusnog liječenja. I dok broj CD4+ T stanica daje podatke o trenutnom imunološkom stanju bolesnika, razina RNK HIV-a predviđa što će se u bliskoj budućnosti dogoditi s brojem CD4+ stanica a time predviđa i kliničku prognozu. Mjerenja razina RNK HIV-a u plazmi trebala bi se učiniti u vrijeme dijagnoze infekcije HIV-om te svaka 3 do 4 mjeseca nakon toga, u neliječenih bolesnika. Mjerenje RNK HIV-a u plazmi također je korisno pri donošenju odluka o antiretrovirusnom liječenju (vidi dalje). Nakon započinjanja liječenja ili bilo koje promjene liječenja, razine RNK HIV-a bi trebalo nadzirati otprilike svaka 4 mjeseca dok se ne utvrdi učinkovitost liječenja pomoću razvoja nove ustaljene razine RNK HIV-a. Tijekom liječenja, razine RNK HIV-a bi trebalo nadzirati svaka 3-4 mjeseca kako bi se procijenila učinkovitost liječenja.
Osjetljivost HIV virusa na različite antiretrovirusne lijekove u pojedinca može se provjeriti genotipskim ili fenotipskim testovima. Ovi testovi su dobri prilikom pronalaženja onih antiretrovirusnih lijekova koje je određeni bolesnik dobivao u prošlosti. U rukama stručnjaka, uporaba testova otpornosti povećava kratkoročnu sposobnost postizanja oko 0,5-log smanjenja opterećenja virusom, u usporedbi s običnim izmjenjivanjem lijekova samo na osnovi povijesti bolesti. Klinička vrijednost testiranja otpornosti HIV-a prilikom odabira početnog liječenja još se istražuje.
Klinička obilježja infekcije HIV-om
Potpuna rasprava prelazi okvire ovog poglavlja. Glavne kliničke osobine različitih stadija infekcije HIV-om sažete su u nastavku teksta (vidi i Pogl. 173, HPIM-16).
AKUTNI HIV (RETROVIRUSNI) SINDROM
Otprilike 50-70% zaraženih osoba nakon primarne infekcije razvija akutni sindrom. Akutni sindrom nastaje 3-6 tjedana nakon infekcije. Obilježen je vrućicama, upalom ždrijela, artralgijama, mijalgijama, limfadenopatijom, makulopapularnim osipom, mukokutanom ulceracijom, mučninom, povraćanjem, proljevom i aseptičnim meningitisom; traje 1-2 tjedna i povlači se spontano, kako se razvija imunološki odgovor na HIV. Većina će bolesnika nakon toga ući u razdoblje kliničke latencije, premda će neki od njih imati progresivno imunološko i kliničko pogoršanje.
ASIMPTOMATSKA INFEKCIJA
Vremensko razdoblje između infekcije i razvoja bolesti uvelike se razlikuje, no medijan trajanja se procjenjuje na 10 godina. Bolest izazvana HIV-om uz aktivno umnažanje virusa za vrijeme tog asimptomatskog razdoblja obično napreduje, a broj CD4+ T stanica pada. Stopa progresije bolesti neposredno korelira s razinama RNK HIV-a u plazmi. Bolesnici s visokim razinama RNK HIV-a napreduju u simptomatsko razdoblje bolesti brže od onih s niskim razinama RNK HIV-a.
SIMPTOMATSKA BOLEST
Simptomi bolesti izazvani HIV-om mogu se razviti u bilo koje doba tijekom infekcije HIV-om. Općenito, spektar bolesti se mijenja kako pada broj CD4+ T stanica. Najteže i po život opasne komplikacije infekcije HIV-om pojavljuju se u bolesnika s brojem CD4+ T stanica < 200/μL. Oko 60% smrtnih slučajeva u bolesnika s AIDS-om je neposredno uzrokovano nekom drugom infekcijom, s bakterijskim infekcijama na vodećem mjestu. Sve u svemu, klinički spektar bolesti izazvane HIV-om se neprekidno mijenja kako bolesnici žive dulje a razvijaju se novi i bolji pristupi liječenju i profilaksi oportunističkih infekcija. Ključni element pri liječenju primarnih i sekundarnih simptomatskih komplikacija bolesti izazvane HIV-om je postizanje dobrog nadzora nad umnožavanjem HIV-a putem primjene kombinacije antiretrovirusnih lijekova i uvođenja primarne i sekundarne profilakse prema indikacijama. Glavni klinički sindromi koji se viđaju u simptomatskom stadiju infekcije HIV-om su sažeti u nastavku.
- Perzistentna generalizirana limfadenopatija: Opipljivo povećanje limfnih čvorova na dva ili više ekstraingvinalna mjesta koje traje >3 mjeseca bez drugog objašnjenja osim infekcije HIV-om. U mnogih će bolesnika doći do progresije bolesti.
- Opći simptomi: Vrućica trajanja >1 mjeseca, neželjeni gubitak težine >10% od početne, proljev trajanja >1 mjeseca bez objašnjivog uzroka.
- Neurološke bolesti: Najčešća je HIV encefalopatija (AIDS dementia complex); ostale neurološke komplikacije uključuju oportunističke infekcije, primarni limfom CNS-a, Kaposijev sarkom CNS-a, aseptični meningitis, mijelopatiju, perifernu neuropatiju i miopatiju.
- Sekundarne zarazne bolesti: Najčešća oportunistička infekcija je P. carinii pneumonija, koja se zbiva u oko 80% osoba tijekom njihove bolesti. Ostali česti uzročnici su CMV (korioretinitis, kolitis, pneumonitis, adrenalitis), Candida albicans (mliječica usne šupljine, ezofagitis), M. avium intracellulare (lokalizirana ili diseminirana infekcija), M. tuberculosis, Cryptococcus neoformans (meningitis, diseminirana bolest), Toxoplasma gondii (encefalitis, intracerebralne promjene u obliku mase), herpes simplex virus (teške mukokutane promjene, ezofagitis), proljev izazvan s Cryptosporidium spp. ili Isospora belli, bakterijski uzročnici (osobito u pedijatrijskim slučajevima).
- Sekundarne novotvorine: Kaposijev sarkom (kožni i visceralni, burnijeg tijeka nego u bolesnika koji nisu zaraženi HIV-om), novotvorine limfatičnog tkiva (osobito B stanični limfomi mozga, koštane srži, GI sustava).
- Ostale bolesti: U bolesnika zaraženih HIV-om može se vidjeti niz za organ specifičnih sindroma, ili u vidu primarnih manifestacija infekcije HIV-om ili u vidu komplikacija liječenja.
(Vidi Pogl. 173, HPIM-16)
LIJEČENJE
Opći principi postupanja s bolesnicima obuhvaćaju savjetovanje, psihosocijalnu potporu i probir na infekcije, te zahtijevaju široko poznavanje procesa bolesti povezanih s infekcijom HIV-om.
Antiretrovirusno liječenje (Vidi Tbl. 105-1)
Kamen temeljac liječenja infekcije HIV-om je kombinacija antiretrovirusnog liječenja ili HAART. U produljenju trajanja života, kao i u poboljšanju kvalitete života bolesnika s infekcijom HIV-om, važna je sastavnica supresija umnažanja HIV-a. Međutim, nekim važnim pitanjima vezanim s liječenjem bolesti izazvane HIV-om nedostaju konačni odgovori. Među njima su pitanja o tome kada treba započeti s antiretrovirusnim liječenjem, koji je najbolji HAART protokol, kada bi se određeni protokol trebalo mijenjati te, kad se promjena učini, koje bi lijekove u protokolu trebalo zamijeniti. Lijekovi koji su trenutno odobreni za liječenje infekcije HIV-om navedeni su u Tbl. 105-1. Ovi lijekovi spadaju u tri glavne skupine: oni koji inhibiraju enzim virusnu reverznu transkriptazu, oni koji inhibiraju enzim virusnu proteazu i oni koji inhibiraju ulazak virusa. Prilikom primjene ovih lijekova moraju se uzeti u obzir brojne interakcije među lijekovima (vidi Tbl. 173-21, u HPIM-16). Jedna od glavnih poteškoća s kojom je došlo do susreta prilikom široke primjene HAART protokola bio je sindrom hiperlipidemije i preraspodjele masti koji se često naziva lipodistrofični sindrom (Pogl. 173, HPIM-16).
Analozi nukleozidaOni bi se smjeli primjenjivati samo u kombinaciji s drugim antiretrovirusnim lijekovima. Jedina je iznimka primjena zidovudina kao monoterapije za sprječavanje prijenosa HIV-a od majke na dijete, kada majci na osnovi stadija njezine bolesti nije potrebno antiretrovirusno liječenje (vidi Pogl. 173, HPIM-16). Najčešća je primjena zajedno s drugim analogom nukleozida, ne-nukleozidnim inhibitorom reverzne transkripataze ili inhibitorom proteaze (vidi dalje).
Ne-nukleozidni inhibitori reverzne transkriptazeOvi lijekovi ometaju funkciju reverzne transkriptaze HIV-a 1 vežući se za regije izvan aktivnog mjesta i uzrokujući konformacijske promjene enzima koje ga čine neaktivnim. Ovi su lijekovi vrlo snažni; međutim, kad se rabe u vidu monoterapije, izazivaju brzo nastajanje mutanata otpornih na lijek. Za kliničku su primjenu trenutno dostupna tri člana ove skupine, nevirapin, delavirdin i efavirenz. Ovi se lijekovi odobravaju za primjenu u kombinaciji s drugim antiretrovirusnim lijekovima.
Inhibitori proteaze Ovi lijekovi su snažni i selektivni inhibitori enzima proteaze HIV-a 1 i aktivni su u nanomolarnim količinama. Na žalost, kao što je slučaj i s inhibitorima ne-nukleozidne reverzne transkriptaze, njihova je snaga popraćena brzim nastankom otpornih izolata, kad se rabe u vidu monoterapije. Zbog toga bi se inhibitori proteaze trebali primjenjivati samo u kombinaciji s drugim antiretrovirusnim lijekovima.
Inhibitori ulaska HIV-a Najnovija skupina antiretrovirusnih lijekova su inhibitori ulaska. Ovi lijekovi ometaju vezanje HIV-a na njegov receptor ili koreceptor ili ometaju proces spajanja. Trenutno je u fazi kliničkog ispitivanja niz malih molekula koje se vežu za koreceptore HIV-a. Prvi lijek iz ove skupine koji će se odobriti je inhibitor spajanja enfuvirtid.
Izbor strategije antiretrovirusnog liječenja
Veliki broj dostupnih antiretrovirusnih lijekova zajedno s relativno malim brojem završenih kliničkih istraživanja, čine pitanje antiretrovirusnog liječenja jednim od prijepornijih pri liječenju bolesnika zaraženih HIV-om.
Principe liječenja zaraze HIV-om oblikovala je skupina koju sponzorira U.S. Department of Health and Human Services (Tbl. 105-2). Prilikom odlučivanja o liječenju u obzir se mora uzeti činjenica kako se radi o kroničnoj infekciji i kako, uz trenutno dostupne HAART protokole iskorjenjivanje HIV-a vjerojatno nije moguće. Stoga, liječenje infekcije HIV-om neposredno nakon postavljanja dijagnoze možda nije mudro, a odluke o liječenju moraju uzimati u obzir ravnotežu između opasnosti i povoljnih učinaka. U ovom je trenutku razumno započeti s antiretrovirusnim liječenjem kod svakoga s akutnim HIV sindromom; kod bolesnika s asimptomatskom infekcijom i brojem CD4 < 350/μL ili s >50.000 kopija/ml RNK HIV-a. Osim toga, kod nezaraženih se osoba neposredno nakon visokorizičnog izlaganja HIV-u može primijeniti liječenje u trajanju od 4 tjedna (vidi dalje).
Kad se u početku liječenja donese odluka, liječnik mora odlučiti koje će lijekove primijeniti u početnom protokolu. Dvije mogućnosti koje se danas najčešće primjenjuje za početno liječenje su: dva analoga nukleozida (od kojih je jedan obično lamivudin) u kombinaciji s inhibitorom proteaze; ili dva analoga nukleozida i ne-nukleozidni inhibitor reverzne transkriptaze. Trenutno ne postoje jasni podaci na kojima se zasniva razlika ovih dvaju pristupa. Nakon početka liječenja može se očekivati 1-log (desetostruko) smanjenje RNK HIV-a u plazmi unutar 1-2 mjeseca te konačno pad RNK HIV-a u plazmi na < 50 kopija/ml. Također bi trebalo doći do porasta broja CD4+ T stanica od 100–150/μL. Mnogi liječnici smatraju kako je neuspjeh u postizanju takvog ishoda indikacija za promjenu liječenja. Drugi razlozi za promjenu liječenja navedeni su u Tbl. 105-3. Prilikom promjene liječenja zbog neuspjeha, važno je pokušati napraviti protokol s barem dva nova lijeka. U bolesnika kod kojih se promjena radi zbog toksičnosti lijeka, razumno je promijeniti samo jedan lijek.
Liječenje sekundarnih infekcija i novotvorina
Specifično za pojedine infekcije i novotvorine (vidi Pogl. 173, u HPIM-16).
Profilaksa sekundarnih infekcija (Tbl. 173-11, HPIM-16) Primarna profilaksa je jasno indicirana za P. carinii pneumoniju (osobito kad broj CD4+ T stanica padne na < 200 stanica/μL), infekciju M. avium kompleksom, i infekcije s M. tuberculosis u bolesnika s pozitivnim PPD testom ili anergijom ako postoji povećana opasnost od tuberkuloze. Svim bolesnicima s brojem CD4+ T stanica >200/μL se općenito preporučuje cijepljenje protiv gripe i pneumokoknim polisaharidnim cjepivom (vidi Tbl. 173-11, HPIM-16). Sekundarna je profilaksa, kad je dostupna, indicirana za praktički svaku infekciju koju dobivaju bolesnici zaraženi HIV-om.
HIV i zdravstveni radnik
Za zdravstvene radnike postoji mala, ali određena opasnost dobivanja infekcije HIV-om zbog izloženosti ubodima igle, izlaganja velikih površina sluznice ili otvorenih rana izlučevinama ili krvnim derivatima HIV-om zaraženih bolesnika. Opasnost od prijenosa HIV-a nakon uboda u kožu predmetom zagađenim krvlju osobe s dokazanom infekcijom HIV-om je oko 3%, u usporedbi s 20-30%-tnom opasnošću od hepatitisa B kod sličnog zbivanja. Uloga antiretrovirusnih lijekova pri postekspozicijskoj profilaksi još je dvojbena. Međutim, radna skupina U.S. Public Health Service preporučuje da se kemoprofilaksa primijeni što je prije moguće nakon profesionalnog izlaganja. I dok točan protokol ostaje predmetom rasprave, naputci U.S. Public Health Service preporučuju primjenu (1.) kombinacije dva analoga nukleozida reverzne transkriptaze tijekom 4 tjedna, prilikom rutinskog izlaganja, ili (2.) kombinaciju dva nukleozidna analoga reverzne transkriptaze plus treći lijek tijekom 4 tjedna u slučajevima visokorizičnih, ili na bilo koji način kompliciranih izlaganja. Većina kliničara u svim slučajevima kad je donesena odluka o liječenju, primjenjuje drugi protokol. Bez obzira na to koji se protokol rabi, liječenje treba započeti što je prije moguće nakon izlaganja.
Najbolja strategija je prevencija izlaganja a uključuje opće mjere predostrožnosti i odgovarajuće postupanje s iglama i drugim zagađenim predmetima.
Prijenos TB je druga moguća opasnost za sve zdravstvene radnike, uključujući i one koji se bave bolesnicima zaraženima HIV-om. Svi bi radnici morali znati svoj PPD status, kojeg treba provjeravati svake godine.
Cjepiva
Razvoj sigurnog i učinkovitog cjepiva protiv HIV-a trenutno je predmet aktivnog istraživanja. Opsežno istraživanje na životinjama je u tijeku a u ljudi su započeta klinička ispitivanja mogućih cjepiva.
Prevencija
Osnove u naporima za prevenciju infekcije HIV-om i dalje ostaju obrazovanje, savjetovanje i promjene ponašanja. Premda je apstinencija apsolutni način prevencije spolnog prijenosa, drugi pristupi, uključuju postupke "sigurnog seksa" poput uporabe prezervativa zajedno sa spermicidom nonoksinolom-9. Vrlo je važno izbjegavanje korištenja iste igle u intravenskih narkomana. Ako je moguće, HIV pozitivne žene ne bi trebale dojiti, jer se virus tim putem može prenijeti djetetu.
Literatura
Opširnije vidi u Fauci AS, Lane HC: Bolesti izazvane humanim virusom imunodeficijencije (HIV-om): AIDS i slični poremećaji, Pogl. 173, HPIM-16.
TABLICA 105-1 Antiretrovirusni lijekovi koji se rabe za liječenje zaraženih HIV-oma
|
Antiretrovirusni lijekovi koji se rabe za liječenje zaraženih HIV-oma
|
|
Lijek
|
Indikacija
|
Doza u kombinaciji
|
Podaci koji podupiru primjenu
|
Toksičnost
|
|
INHIBITORI REVERZNE TRANSKRIPTAZE
|
|
Zidovudin (AZT, azidotimidin, Retrovir, 3′azido-3′-deoksitimidin)
|
Liječenje infekcije HIV-om u kombinaciji s drugim antiretrovirusnim lijekovima
|
200 mg svakih 8 h ili 300 mg 2x/dan
|
19 naprama 1 smrtnom slučaju u originalnom, s placebom kontroliranom istraživanju u 281 bolesnika s AIDS-om ili ARC-om. Usporena progresija u AIDS kod bolesnika s brojem CD4+ T stanica < 500/ μL, n = 2051
|
Anemija, granulocitopenija, miopatija, laktacidoza, hepatomegalija sa steatozom, glavobolja, mučnina
|
|
|
Prevencija prijenosa HIV-a s majke na fetus
|
|
U trudnica s brojem CD4+ T stanica ≥200/μL, AZT PO s početkom od 14 do 34 tjedna gestacije IV primjena lijeka tijekom poroda plus primjena AZT PO u djeteta tijekom 6 tj. smanjen prijenos HIV-a za 67,5% (od 25,5% do 8,3%), n = 363
|
|
|
Didanozin (Videx, Videx EC, ddI, dideoksinozin, 2′,3′-dideoksinozin)
|
Za liječenje infekcija HIV-om u kombinaciji s drugim antiretrovirusnim lijekovima
|
Puferirani: Za postizanje odgovarajućeg puferskog djelovanja na želučanu kiselinu potrebne su 2 tablete; treba se uzimati na prazan želudac
≥60 kg: 200 mg 2x/dan
< 60 kg: 125 mg 2x/dan
Film tablete: ≥60 kg: 400 mg 4x/dan < 60 kg: 250 mg 4x/dan
|
Klinički bolji od AZT-a u vidu monoterapije u 913 bolesnika prethodno liječenih AZT-om. Klinički bolji od AZT-a i usporediv s AZT + ddI te AZT + ddC u 1067 bolesnika koji nisu prethodno primali AZT, s brojem CD4+ T stanica od 200–500/μL
|
Pankreatitis, periferna neuropatija, poremećaji testova jetrene funkcije, laktacidoza, hepatomegalija sa steatozom
|
|
Zalcitabin (ddC, HIVID, 2′3′-dideoksicitidin)
|
U kombinaciji s drugim antiretrovirusnim lijekovima za liječenje infekcije HIV-om
|
0,75 mg 3x/dan
|
Klinički lošiji od monoterapije AZT-om za početno liječenje. Klinički jednako dobar kao i ddI u uznapredovaloj bolesti u bolesnika s nepodnošenjem AZT-a. U kombinaciji s AZT-om bio je klinički bolji od AZT-a samog u bolesnika s AIDS-om ili brojem CD4+ T stanica < 350/μL
|
Periferna neuropatija, pankreatitis, laktacidoza, hepatomegalija sa steatozom, ulkusi u usnoj šupljini
|
|
Stavudin (d4T, Zerit, 2′3′-didehidro-3′-dideoksitimidin)
|
Liječenje bolesnika zaraženih HIV-om u kombinaciji s drugim antiretrovirusnim lijekovima
|
≥60 kg: 40 mg 2x/dan
< 60 kg: 30 mg 2x/dan
|
Bolji od AZT-a s obzirom na promjene broja CD4+ T stanica u 359 bolesnika koji su primali AZT ≥24 tj. Nakon 12 tj. randomizacije, broj CD4+ T stanica se smanjio u s AZT liječenoj kontrolnoj skupini u prosjeku za 22/μL, dok se u bolesnika liječenih stavudinom povećao za prosječno 22/μL
|
Periferna neuropatija, pankreatitis, laktacidoza, hepatomegalija sa steatozom, uzlazna mišićna slabost, lipodistrofija
|
|
Lamivudin (Epivir, 2′3′-dideoksi-3′-tiacitidin, 3TC)
|
U kombinaciji s drugim antiretrovirusnim lijekovima za liječenje infekcije HIV-om
|
150 mg 2x/dan
300 mg 4x/dan
|
Bolji od samog AZT-a s obzirom na promjene broja CD4 u 495 bolesnika koji nisu prije primali zidovudin i 477 bolesnika koji su ga primali. Sveukupni broj CD4+ T stanica u zidovudinskoj skupini bio je na početnoj vrijednosti nakon 24 tj., dok je u skupini liječenoj zidovudinom plus lamivudinom on bio za 10–50 stanica/μL iznad početne vrijednosti. 54%-tno smanjenje progresije u AIDS/smrt u usporedbi sa samim AZT-om
|
|
|
Emtricitabin (FTC, Emtriva)
|
U kombinaciji s drugim antiretrovirusnim lijekovima za liječenje infekcije HIV-
|
200 mg 4x/dan
|
Usporediv s d4T u kombinaciji s ddI efavirencom u 571 bolesnika koji prethodno nisu liječeni. Sličan 3TC-u u kombinaciji s 2DV ili d4T + NNRT1 ili PI u 440 bolesnika koji su nakon barem 12 tjedana na kuri 3TC-om bili dobro.
|
|
|
Abakavir (Ziagen)
|
Za liječenje infekcija HIV-om u kombinaciji s drugim antiretrovirusnim lijekovima
|
300 mg 2x/dan
|
Abakavir + AZT + 3TC jednaki su indinaviru + AZT + 3TC s obzirom na supresiju količine virusa (oko 60% u svakoj skupini, s < 400 HIV RNK kopija/mL plazme) i povećanju broja CD4 stanica oko 100/μL u svakoj skupini) nakon 24 tjedna
|
Reakcija preosjetljivosti (može biti smrtonosna), vrućica, osip, mučnina, povraćanje, malaksalost ili zamor i gubitak apetita
|
|
Tenofovir (Viread)
|
Za primjenu u kombinaciji s drugim antiretrovirusnim lijekovima kad je liječenje indicirano
|
300 mg 4x/dan
|
Smanjenje od oko 0,6 log razina HIV-1 RNK kad je dodan postojećem protokolu, u već liječenih bolesnika
|
Moguća nefrotoksičnost
|
|
Delavirdin (Rescriptor)
|
Za primjenu u kombinaciji s odgovarajućim antiretrovirusnim lijekovima kad je potrebno liječenje
|
400 mg 3x/dan
|
Delavirdin + AZT su bolji od samog AZT-a u pogledu supresije količine virusa nakon 52 tjedna
|
Kožni osip, poremećaji testova funkcije jetre
|
|
Nevirapin
(Viramune)
|
U kombinaciji s drugim antiretrovirusnim lijekovima za liječenje progresivne infekcije HIV-om
|
200 mg/dan × 14 dana, zatim 200 mg 2x/dan
|
Povećanje broja CD4+ T stanica, smanjenje HIV RNK kad se primjenjuje u kombinaciji s nukleozidima
|
Kožni osip, hepatotoksičnost
|
|
Efavirenc (Sustiva)
|
Za liječenje HIV infekcije u kombinaciji s drugim antiretrovirusnim lijekovima
|
600 mg prije spavanja
|
Efavirenc + AZT + 3TC su usporedivi s indinavirom + AZT + 3TC s obzirom na supresiju količine virusa (u skupini liječenoj efavirencom veći postotak je dosegao količinu virusa od < 50 kopija/ml; međutim je stopa prekida liječenja u skupini liječenoj indinavirom bila neočekivano visoka, zbog čega je u većini slučajeva došlo do "neuspjeha" liječenja) i povećanje broja CD4 stanica (oko 140/μL u svakoj skupini) nakon 24 tjedna
|
Osip, depresija, porast parametara jetrene funkcije, omamljenost, nenormalni snovi, depresija
|
|
INHIBITORI PROTEAZE
|
|
Sakvinavir mesilat (Invirase—tvrda gel kapsula)
|
U kombinaciji s drugim antiretrovirusnim lijekovima kad je potrebno liječenje
|
600 mg svakih 8 h
|
Povećanje broja CD4+ T stanica, smanjenje HIV RNK najizraženije u kombinaciji s ddC. 50% smanjenje kod prvog očitovanja AIDS-a ili smrti u kombinaciji s ddC, u usporedbi sa samo bilo kojim od njih
|
Proljev, mučnina, povraćanje, glavobolje, hiperglikemija, preraspodjela masnog tkiva, poremećaji lipida
|
|
(Fortovaz—meka gel kapsula)
|
Za primjenu u kombinaciji s drugim antiretrovirusnim lijekovima kad je potrebno liječenje
|
1200 mg 3x/dan
|
Smanjenje stope smrtnosti i očitovanja AIDS-a u bolesnika koji su primali pripravak u obliku tvrdog gela u kombinaciji s ddC
|
Proljev, mučnina, bol u trbuhu, glavobolje, hiperglikemija, preraspodjela masnog tkiva, poremećaji lipida
|
|
Ritonavir (Norvir)
|
U kombinaciji s drugim antiretrovirusnim lijekovima za liječenje infekcije HIV-om kad je potrebno liječenje
|
600 mg 2x/dan
|
Smanjenje kumulativne incidencije kliničke progresije ili smrti od 34 do 17% u bolesnika s brojem CD4+ T stanica < 100/μL liječenih prosječno 6 mjeseci
|
Mučnina, bol u trbuhu, hiperglikemija, preraspodjela masnog tkiva, poremećaji lipida, može promijeniti razine mnogih drugih lijekova, uključujući sakinavir
|
|
Indinavir sulfat (Crixivan)
|
Za liječenje HIV infekcije u kombinaciji s drugim antiretrovirusnim lijekovima kad je potrebno antiretrovirusno liječenje
|
800 mg svakih 8 h
|
Povećanje broja CD4+ T stanica za 100/μL i smanjenje razina HIV RNK za 2-log, kad se daje sa zidovudinom i lamivudinom. Smanjenje opasnosti od progresije u AIDS i smrt za 50%, kad se daje sa zidovudinom i lamivudinom u usporedbi sa samo zidovudinom i lamivudinom
|
Nefrolitijaza, indirektna bilirubinemija, hiperglikemija, preraspodjela masnog tkiva, poremećaji lipida
|
|
Nelfinavir mesilat (Viracept)
|
Za liječenje HIV infekcije u kombinaciji s drugim antiretrovirusnim lijekovima kad je potrebno antiretrovirusno liječenje
|
750 mg 3x/dan ili 1250 mg 2x/dan
|
Smanjenje HIV RNK za 2,0-log kad se daje u kombinaciji sa stavudinom
|
Proljev, mekana stolica, hiperglikemija, preraspodjela masnog tkiva, poremećaji lipida
|
|
Amprenavir (Agenerase)
Fosamprenavir (Lexiva)
|
U kombinaciji s drugim antiretrovirusnim lijekovima, za liječenje infekcije HIV-om
|
1200 mg 2x/dan ili 600 mg 2x/dan + ritonavir 100 mg 2x/dan ili 1200 mg svaki dan + ritonavir 200 mg svaki dan
1400 mg 2x/dan ili 700 mg 2x/dan + ritonavir 100 mg 2x/dan
|
U do tada neliječenih bolesnika, amprenavir + AZT + 3TC su bolji od AZT + 3TC s obzirom na supresiju količine virusa (53% naprama 11% s < 400 HIV RNK kopija/ml plazme nakon 24 tjedna). Odgovori CD4+ T stanica slični u liječenim skupinama. U već liječenih bolesnika, amprenavir + NRTI slično indinaviru + NRTI s obzirom na supresiju količine virusa (43% naprama 53% s < 400 HIV RNK kopija/ml plazme nakon 24 tjedna). Odgovori CD4+ T stanica bolji u skupini liječenoj indinavirom + NRTI
|
Mučnina, povraćanje, proljev, osip, oralne parestezije, porast parametara jetrene funkcije, hiperglikemija, preraspodjela masti, poremećaji lipida
|
|
Lopinavir/ritonavir (Kaletra)
|
Za liječenje infekcije HIV-om u kombinaciji s drugim antiretrovirusnim lijekovima
|
400 mg/100 mg 2x/dan
|
Pri liječenju bolesnika koji do tada nisu ničim liječeni, lopinavir/ritonavir + d4T + 3TC bolji od nelfinavira + d4T + 3TC s obzirom na supresiju količine virusa (79% naprama 64% s < 400 HIV RNK kopija/ml nakon 40 tjedana). CD4+ T stanice se povećavaju slično u obje skupine.
|
Proljev, hiperglikemija, preraspodjela masti, poremećaji lipida
|
|
Atazanavir (Reyataz)
|
Za liječenje infekcije HIV-om u kombinaciji s drugim antiretrovirusnim lijekovima
|
400 mg na dan ili 300 mg na dan + ritonavir 100 mg na dan kad se daje s efavirencom
|
Usporediv s efavirencom kad se daje u kombinaciji s AZT + 3TC u istraživanju 810 do tada neliječenih bolesnika. Usporediv s nelfinavirom, kad se daje u kombinaciji s d4T + 3TC u istraživanju 467 do tada neliječenih bolesnika.
|
Hiperbilirubinemija, produljenje PR-intervala, mučnina, povraćanje, hiperglikemija, preraspodjela masti
|
|
INHIBITOR SPAJANJA
|
|
Enfuvirtid (Fuzeon)
|
U kombinaciji s drugim lijekovima pri liječenju već prije liječenih bolesnika s dokazima umnažanja HIV-a 1, unatoč trajanju antiretrovirusnog liječenja
|
90 mg SC 2x/dan
|
U liječenju već liječenih bolesnika bolji od placeba kad se uvodi kod nove, poboljšane situacije (37% naprama 16% s < 400 HIV RNK kopija/ml nakon 24 tjedna; + 71 naprama + 35 CD4+ T stanica nakon 24 tjedna)
|
Lokalne reakcije na injekciju, reakcije preosjetljivosti, povećana stopa bakterijske pneumonije
|
a Svi lijekovi navedeni u ovoj tablici su odobreni za uporabu.
Tumač: ARC = kompleks srodan AIDS-u; NRTIs = ne-nukleozidni inhibitori reverzne transkriptaze.
TABLICA 105-2 Principi liječenja infekcije HIV-om
|
Principi liječenja infekcije HIV-om
|
- Trajna replikacija HIV-a dovodi do oštećenja imunološkog sustava i progresije u AIDS.
- Razine HIV RNK ukazuju na opseg replikacije HIV-a i stopu uništenja CD4+ T stanica. Broj CD4+ T stanica pokazuju trenutni stupanj kompetencije imunološkog sustava.
- Stope progresije bolesti se razlikuju od osobe do osobe a odluke o liječenju se trebaju individualizirati, na osnovi razina HIV RNK u plazmi i broja CD4+ T stanica.
- Cilj liječenja je maksimalna supresija replikacije virusa, što je veća supresija, manje je vjerojatna pojava na lijek otpornih oblika.
- Najučinkovitije strategije liječenja uključuju istodobno započinjanje kombinacija učinkovitih anti-HIV lijekova s kojima se bolesnik nije prije liječio i na koje ne postoji križana otpornost s antiretrovirusnim lijekovima koje je bolesnik već dobivao.
- Antiretrovirusni lijekovi rabljeni u kombinacijama trebaju se primjenjivati prema optimalnom rasporedu i doziranju.
- Broj dostupnih lijekova je ograničen. Svaka odluka o antiretrovirusnom liječenju ima dugoročan učinak na buduće mogućnosti za bolesnika.
- Žene bi trebale dobiti optimalno antiretrovirusno liječenje bez obzira na trudnoću.
- Ista se načela odnose na djecu i odrasle. Liječenje djece zaražene HIV-om uključuje jedinstvena farmakološka, virološka i imunološka razmatranja.
- Bolesnikova suradnja je važan dio osiguravanja maksimalnog učinka određenog protokola. Što je protokol jednostavniji, bolesniku je lakše provoditi ga.
|
Izvor: Prilagođeno iz Principles of Therapy of HIV Infection, USPHS and the Henry J. Kaiser Family Foundation.
TABLICA 105-3 Indikacije za promjenu antiretrovirusnog liječenja u bolesnika zaraženih HIV-oma
|
Indikacije za promjenu antiretrovirusnog liječenja u bolesnika zaraženih HIV-oma
|
|
Nakon 4 tjedna od početka liječenja pad HIV RNK u plazmi manji od 1-log
Najveći mogući postignuti porast (definiran kao 3-struki ili veći) od najniže razine HIV RNK u plazmi koji se ne može pripisati trenutnoj infekciji, cijepljenju ili metodologiji izvođenja testa
Stalni pad broja CD4+ T stanica
Kliničko pogoršanje
Nuspojave
|
a Općenito govoreći, promjena bi se trebala sastojati od uvođenja barem 2 lijeka koja bi trebala biti učinkovita u dotičnog bolesnika. Iznimka je, promjena poduzeta zbog toksičnosti, pa je u tom slučaju razumna zamjena samo jednog lijeka.
Izvor: Guidelines for the Use of Antiretroviral Agents in HIV-Infected dults and Adolescents. USPHS.