KARCINOM JEDNJAKA
2015. godine u SAD-u je bilo 16.980 novootkrivenih bolesnika, a 15.590 bolesnika je umrlo; manje je učestao u žena. Incidencija je najveća u pojedinim područjima područjima Kine, Irana, Afganistana, Sibira i Mongolije. U SAD-u crnci češće obolijevaju nego bijelci. Obično se javlja u šestom desetljeću ili kasnije. Petogodišnje preživljavanje je <10% obzirom da se većina slučajeva otkriva u uznapredovalom stadiju.
Patologija
Na planocelularni karcinom otpada 20% slučajeva, najčešći je u gornje dvije trećine; oko 75% je adenokarcinom, obično u distalnoj trećini, a nastaje u području metaplazije cilindičnog epitela (Barretov jednjak), iz žljezdanog tkiva ili izravnim širenjem proksimalnog adenokarcinoma želuca. Limfom i melanom su rijetki. 5% svih ezofagealnih tumora nastaje u gornjoj trećini, 20% u srednjoj i oko 75% u donjoj trećini. Oko 15% tumora je HER/neu (HER2) pozitivno.
Čimbenici rizika
Glavni čimbenici rizika za planocelularni karcinom su: prekomjerno uživanje alkohola, pušenje (kombinacija je sinergistična), a ostali rizici su: unos lužine i strikutra jednjaka, izloženost zračenju, rak glave i vrata, ahalazija, pušenje opijata, Plumer-Vinsonov sindrom, tiloza, kronična konzumacija izrazito vrućeg čaja, manjak vitamina A, cinka, molibdena. Za nastanak adenokarcinoma, najvažniji su rizični čimbenici Barretov jednjak, kronični gastroezofagealni refluks i debljina.
Klinička slika
Progresivna disfagija (najprije za čvrstu hranu, potom i za tekućinu), brzi gubitak tjelesne težine, bol u prsima (zbog širenja u sredogruđu), odinofagija, plućna aspiracija (opstrukcija, traheoezofagealna fistula), promuklost (paraliza laringealnog živca), hiperkalcijemija (hipersekrecija peptida srodnog parathormonu iz stanica planocelularnog karcinoma); rjeđe krvarenje, katkad ozbiljno; fizikalni pregled često je bez osobitosti.
Dijagnoza
Gutanje dvostrukog barijskog kontrasta je korisna početna pretraga kod disfagije. Fleksibilna ezofagogastroskopija je najosjetljivija i najspecifičnija pretraga. Dijagnozu potvrđuje pozitivan patohistološki nalaz u bioptatu (endoskopska biopsija) i citološkom uzorku dobivenom četkanjem sluznice (niti jedan nalaz sam nije dovoljno osjetljiv). CT i endoskopski ultrazvuk su vrijedne pretrage za procjenu lokalne proširenosti i širenja u limfne čvorove. PET sken također kao opcija, za određivanje stanja medijastinalnih čvorova i udaljenih metastaza.
LIJEČENJE KARCINOM JEDNJAKA
Kirurška resekcija je uspješna u samo 40% slučajeva. Povezana je s visokim postotkom komplikacija (fistula, apsces, aspiracija). Planocelularni karcinom: kirurška resekcija nakon kemoterapije [5-fluorouracil (5-FU), cisplatina] i radioterapija produžuju preživljavanje i mogu poboljšati stopu izlječenja. Adenokarcinom: kurativna resekcija je rijetko moguća; <20% bolesnika s operabilnim tumorom preživi 5 godina. Palijativne mjere uključuju lasersku ablaciju, mehaničku dilataciju, radioterapiju i endoluminalnu protezu radi premoštenja tumora. Gastrostoma ili jejunostoma su često potrebne zbog nutritivne potpore. Preoperativna kemoterapija uz popratnu radioterapiju je donekle efektivnija, ali toksičnija.
KARCINOM ŽELUCA
Incidencija je najveća u Japanu, Kini, Čileu, Irskoj; diljem svijeta incidencija opada, u SAD-u za osam puta u zadnjih 60 godina; 2015. godine bilo je 24.590 novih i 10.720 smrtnih slučajeva. Omjer muškog i ženskog spola je 2:1. Incidencija je najveća u 6. i 7. desetljeću; ukupno petogodišnje preživljavanje je <15%.
Čimbenici rizika
Incidencija je povećana u nižim društveno-ekonomskim skupinama. Ispitivanja doseljenika i njihovih potomaka ukazuju na važan utjecaja okoliša. Nekoliko je prehrambenih čimbenika u korelaciji s povećanom incidencijom: nitrati, dimljena hrana, previše zasoljena hrana. Obzirom na povećanu incidenciju u prvih rođaka oboljelih, pretpostavljena je genetska komponenta. Drugi čimbenici rizika su: atrofični gastritis, infekcija s Helicobacter pylori, Billroth II gastrektomija, gastrojejunostoma, adenomatozni želučani polipi, perniciozna anemija, hiperplastični želučani polipi (posljednja dva uzroka su povezana s atrofičnim gastritisom), Ménétrierova bolest; rizik je neznatno povećan u osoba krvne grupe A.
Patologija
Adenokarcinom u 85% slučajeva; obično fokalni (polipoidni, ulcerozni), u dvije trećine slučajeva je na antrumu ili na maloj krivini, često ulcerozni (“intestinalni tip”); rjeđe difuzno infiltrativni (linitis plastica) ili se širi površinski (difuzne lezije češće u mlađih bolesnika; s manjim zemljopisnim varijacijama; imaju izuzetno lošu prognozu); primarno se šire u regionalne limfne čvorove, jetru, peritoneum; sistemsko širenje nije često; postotak limfoma iznosi 15% (u imunokompetentnih bolesnika najčešće se nalazi ekstranodalno), MALT–limfom niskog stupnja malignosti (mucosa-associated lymphoid tissue) ili difuzni agresivni B velikostanični limfom; leiomiosarkom ili gastrointestinalni stromalni tumor (GIST) su rijetki.
Klinička slika
Najčešće se očituje progresivnom nelagodom u gornjem abdomenu, često s gubitkom tjelesne težine, anoreksijom, mučninom; često je akutno ili kronično GI krvarenje (ulceracija sluznice); disfagija (smješten u kardiji); povraćanje (pilorična i proširena bolest); rana sitost; pregledom se često ne otkriva u ranom stadiju; kasnije su abdominalna osjetljivost, bljedilo i kaheksija uobičajeni znaci; palpabilna masa nije uobičajen nalaz; metastatsko širenje se može manifestirati hepatomegalijom, ljevostranom supraklavikularnom ili skalenskom adenopatijom, periumbilikalnom, ovarijskom ili prerektalnom tvorbom (Blummerov greben), subfebrilitetom, kožnim promjenama (čvorovi, dermatomiozitis, acanthosis nigricans ili multiple seboroične keratoze). Laboratorijski nalazi: sideropenična anemija u dvije trećine bolesnika, skrivena krv u stolici u 80%; rijetko udružen s pancitopenijom i mikroangiopatskom hemolitičnom anemijom (zbog infiltracije koštane srži), leukemoidnom reakcijom, migrirajućim tromboflebitisom ili acanathosis nigricans.
Dijagnoza
Pasaža dvostrukim barijevim kontrastom je korisna, ali je zamjenjena značajno osjetljivijom i specifičnijom ezofagogastroduodenoskopijom i CT-om u određivanju stadija i resektabilnosti; patohistološka potvrda biopsije i citološka analiza uzoraka dobivenih četkanjem sluznice; površinske biopsije manje su osjetljive za limfome (češće submukozno smješteni); važno je razlikovanje dobroćudnih od zloćudnih želučanih ulkusa višestrukim uzimanjem biopsija i kontrolnim endoskopskim pregledima s ciljem dokumentacije cijeljenja ulkusa.
LIJEČENJE KARCINOM ŽELUCA
Adenokarcinom: Samo gastrektomija nudi priliku za izlječenje (samo 1/3 slučajeva). Rijetki tumori ograničeni na sluznicu su operabilni i izlječivi u 80% slučajeva. Dublji prodor i metastaze u limfne čvorove smanjuju petogodišnje preživljavanje na 20% u bolesnika s operabilnim tumorima bez očiglednog metastatskog širenja (Tbl. 71-1). Subtotalna gastrektomija ima sličnu učinkovitost kao i totalna gastrektomija za distalne lezije želuca, ali je morbiditet manji. Nije dokazano da resekcija slezene i dijela gušterače ili radikalno odstranjenje limfnih čvorova poboljšava ishod. Adjuvantna kemoterapija (5-FU/leukovorin) i zračenje nakon primarnog kirurškog zahvata produžuju srednje preživljavanje za 7 mjeseci. Neoadjuvantna kemoterapija epirubicinom, ili docetaxel +cisplatinom i 5-FU ili capecitabinom može dovesti do vraćanja tumora u niži stadij i tako povećati učinkovitost operacije. Palijativno liječenje boli, opstrukcije i krvarenja uključuje operaciju, endoskopsku dilataciju, zračenje, kemoterapiju, te ramucirumab (anti-angiogeno antitijelo).
TABLICA 71-1 ODREĐIVANJE STADIJA KARCINOMA ŽELUCA
|
|
Stadij
|
TNM
|
Obilježja
|
Podaci iz ACS-a
|
|
Broj slučajeva, %
|
5-godišnje preživljenje, %
|
|
0
|
TisN0M0
|
Negativni l. č., ograničen na sluznicu
|
1
|
90
|
|
IA
|
T1N0M0
|
Negativni l. č; zahvaćena lamina propria ili muskularis mukoze
|
7
|
59
|
|
IB
|
T2N0M0
T1N1M0
|
Negativni l. č.; zahvaćena submukoza
|
10
|
44
|
|
IIA
|
T1N2M0
T2N1M0
|
Pozitivni l. č; ne probija stijenku sluznice ili
|
17
|
29
|
|
|
T3N0M0
|
negativni l. č.; probija sluznicu
|
|
|
|
IIB
|
T4aN0M0
T3N1M0
T2N2M0
|
Tm zahvaća serozu (visceralni peritoneum)
|
|
|
|
IIIA
|
T4aN1M0
T3N2M0
T2N3M0
|
Pozitivni l. č.; prodire u muscularis propriae ili proboj kroz stijenku
|
21
|
15
|
|
IIIB
|
T4bN0-N1M0
T4aN2M0
T3N3M0
|
Negativni l. č.; prijanjanje za okolno tkivo;
7 ili više pozitivnih l. č.; prodor u stijenku bez invazije seroze ili okolnih struktura
|
14
|
9
|
|
IIIC
|
T4bN2-3M0
T4aN3M0
|
>3 l. č. pozitivna; prodor u serozu ili okolne strukture
|
|
|
|
IV
|
Bilo koji T
Bilo koji N
M1
|
Pozitivni l. č.; prijanjanje za okolno tkivoUdaljene metastaze
|
30
|
3
|
|
Kratice: ACS = Američko onkološko društvo (American Cancer Society); TNM = tumor-nodus-metastaza.
|
Limfom: MALT-limfom niskog stupnja malignosti je uzrokovan H. pylori infekcijom pa iskorjenjivanje infekcije dovodi do potpunog povlačenja tumora u 50% bolesnika. Ostali dobro odgovaraju na polikemoterapiju koja uključuje ciklofosfamid, doksorubicin, vinkristin, prednizon (CHOP) plus rituksimab. Difuzni limfom velikih stanica može se liječiti ili CHOP protokolom i rituksimabom ili subtotalnom gastrektomijom nakon koje slijedi kemoterapija. Petogodišnje preživljavanje iznosi 50–60%.
Leiomiosarkom: Kirurška resekcija je kurativna u većine bolesnika. Tumori koji izražavaju c-kit tirozin kinazu (CD 117)—GIST—u znatnom broju slučajeva odgovaraju na liječenje imatinib mesilatom.
BENIGNI TUMORI ŽELUCA
Mnogo su rjeđi od malignih tumora želuca; najčešći su hiperplastični polipi, rjeđe adenomi, hamartomi i leiomiomi; 30% adenoma i povremeno hiperplastičnih polipa udruženo je s malignitetom; polipozni sindromi su Peutz-Jeghersov sindrom i obiteljska polipoza (hamartomi ili adenomi); Gardnerov sindrom (adenomi) i Cronkhite-Canada sindrom (cistični polipi). Vidi “Polipi kolona” ispod.
Klinička slika
Obično asimptomatski; katkad se očituju krvarenjem ili nejasnom epigastričnom nelagodom.
LIJEČENJE BENIGNI TUMORI ŽELUCA
Endoskopska ili kirurška ekscizija.
TUMORI TANKOG CRIJEVA
Klinička slika
Rijetki tumori (~5% svih GI neoplazmi); obično se očituju krvarenjem, bolovima u trbuhu, gubitkom tjelesne težine, vrućicom ili crijevnom opstrukcijom (povremenom ili trajnom). Limfomi imaju povećanu incidenciju u bolesnika s glutenskom enteropatijom, Crohnovom bolešću koja zahvaća tanko crijevo, AIDS-om, prethodnom transplantacijom organa, autoimunim poremećajima.
Patologija
Obično su benigni; najčešće adenomi (obično duodenalni), leiomiomi (intramuralni) i lipomi (obično ilealni); 50% malignih tumora čine adenokarcinomi, obično u duodenumu (na ili u blizini ampule Vateri) ili proksimalnom jejunumu, obično se pojavljuju uz benigne adenome. Primarni crijevni limfomi (ne-Hodgkin) na koje otpada oko 25%, pojavljuju se kao žarišne tvorbe (zapadni tip) koje su obično T-stanični limfom udružen s prethodnom celijakijom, ili kao difuzna infiltracija (Mediteranski tip) koji su obično imunoproliferativna bolest tankog crijeva (IPBTC; bolest α-teških lanaca), B stanični MALT-limfom udružen s Campylobacter jejuni infekcijom koja se može očitovati kao crijevna malapsorpcija; karcinoidni tumori (obično asimptomatski) povremeno dovode do krvarenja ili invaginacije crijeva (vidi ispod).
Dijagnoza
Endoskopija i biopsija su najkorisnije za tumore duodenuma i proksimalnog jejunuma. Inače, radiološka kontrastna pretraga barijem je najbolja dijagnostička metoda. Izravno uvođenje kontrasta u tanko crijevo (enterokliza) povremeno prikazuje tumore koji nisu viđeni na rutinskoj radiografiji tankog crijeva. Angiografija (za otkrivanje spleta tumorskih krvnih žila) ili laparotomija često su potrebni za postavljanje dijagnoze. CT se koristi za procjenu proširenosti tumora (osobito limfoma).
LIJEČENJE TUMORI TANKOG CRIJEVA
Kirurška ekscizija; adjuvantna kemoterapija se pokazala korisnom za žarišni limfom. IP IPBTC–imunoproliferativna bolest tankog crijeva je izlječiva polikemoterapijom koja se primjenjuje kod agresivnih limfoma u kombinaciji s oralnim antibioticima (npr. tetraciklinima). Uloga kemoterapije ili zračenja za druge tumore tankog crijeva nije dokazana.
POLIPI KOLONA
TUBULARNI ADENOMI
Nalaze se u ~30% odraslih, imaju peteljku ili se drže za podlogu pa su nepomični; obično asimptomatski; u ~5% slučajeva dovode do skrivenog krvarenja u stolici; mogu dovesti do opstrukcije; ukupni rizik od prelaska u malignom je u korelaciji s veličinom (<2% ako je promjera <1,5 cm; >10% ako je promjera >2,5 cm), a rizik je veći i kod nepomičnih (sesilnih) polipa. U 65% slučajeva nađu se u rektosigmoidnom kolonu. Dijagnoza se postavlja pomoću barijske klizme, sigmoidoskopijom ili kolonoskopijom. Liječenje: Totalna kolonoskopija za otkrivanje sinkronih lezija (u 30% slučajeva); endoskopska resekcija (operacija ukoliko je polip velik ili nedostupan pri kolonoskopiji); kontrolna kolonoskopija svake 2–3 godine.
VILOZNI ADENOMI
Općenito su pri postavljanju dijagnoze veći nego tubularni adenomi; često sesilni; visok rizik od maligniteta (do 30% kada su >2 cm); češći u lijevom kolonu; povremeno udruženi sa sekretornom dijarejom bogatom kalijem. Liječenje: Kao za tubularne adenome.
HIPERPLASTIČNI POLIPI
Asimptomatski; obično slučajan nalaz na kolonoskopiji; rijetko >5 mm; nemaju maligni potencijal. Liječenje nije potrebno.
SINDROMI NASLJEDNE POLIPOZE
Vidi Tbl. 71-2.
TABLICA 71-2 SINDROMI NASLJEDNE POLIPOZE (AUTOSOMNO DOMINANTNI)
|
|
Gastrointestinalni polipozni sindromi
|
|
Sindrom
|
Distribucija polipa
|
Histološki tip
|
Maligni potencijal
|
Pridužene lezije
|
|
Obiteljska adenomatozna polipoza
|
Debelo crijevo
|
Adenom
|
Uobičajen
|
Nema
|
|
Gardnerov sindrom
|
Tanko I debelo crijevo
|
Adenom
|
Uobičajen
|
Osteomi, fibromi, lipomi, epidermoidne ciste, ampularni karcinomi, prirođena hipertrofija epitelnih stanica pigmentnog sloja mrežnice
|
|
Turcotov sindrom
|
Debelo crijevo
|
Adenom
|
Uobičajen
|
Tumori mozga
|
|
Nepolipozni sindrom (Lynchov sindrom)
|
Debelo crijevo (često proksimalni dio)
|
Adenom
|
Uobičajen
|
Tumori endometrija i jajnika
|
|
Peutz-Jeghersov sindrom
|
Tanko i debelo crijevo, želudac
|
Hamartom
|
Rijedak
|
Mukokutana pigmentacija; tumori jajnika, dojke, gušterače i endometrija
|
|
Juvenilna polipoza
|
Tanko i debelo crijevo, želudac
|
Hamartom, rijetko prelazi u adenom
|
Rijedak
|
Razne prirođene abnormalnosti
|
- Obiteljska polipoloza kolona (OPK): Difuzna pankolonska adenomatozna polipoza (do nekoliko tisuća polipa); autosomno dominantno nasljeđe udruženo s delecijom (brisanjem) na genu adenomske polipoze kolona (APC) na 5. kromosomu; karcinom kolona iz maligne degeneracije polipa u 100% slučajeva u dobi do 40 godina. Liječenje: Totalna profilaktična kolektomija ili subtotalna kolektomija sa ileoproktostomom prije dobi od 30 godina; subtotalna resekcija omogućuje izbjegavanje ileostome, ali su nužne učestale proktoskopske kontrole; periodično kolonoskopsko ili radiološki screening braće i sestara te potomaka bolesnika s OPK do dobi od 35 godina; sulindak i drugi nesteroidni protu-upalni lijekovi dovode do povlačenja polipa i koče njihov razvoj.
- Gardnerov sindrom: Varijanta OPK udružena s tumorima mekog tkiva (epidermiodne ciste, osteomi, lipomi, fibromi, dezmoidi). Veća incidencija gastrointestinalnih polipa, ampularnog adenokarcinoma. Liječenje: Kao za OPK; nadzor bolesti tankog crijeva pretragom stolice na skriveno krvarenje nakon kolektomije.
- Turcotov sindrom: Rijetka varijanta OPK udružena s malignim tumorima mozga. Liječenje: Kao za OPK.
- Nepolipozni sindrom: Obiteljski sindrom s rizikom za nastanak karcinoma kolona i do 50%; najviša incidencija u petom desetljeću; povezan s višestrukim primarnim karcinomima (osobito endometrija); autosomno dominantan; nastaje zbog nepotpunog popravka oštećenja na DNK.
- Juvinelina polipoza: Multipli benigni hamartomi kolona i tankog crijeva; crijevno krvarenje je često. Ostali simptomi: abdominalna bol, dijareja, povremeno invaginacija crijeva. Rijetko ponovno nastaju nakon ekscizije; mali rizik za nastanak raka kolona zbog maligne degeneracije razasutih adenomatoznih polipa. Profilaktična kolektomija je sporno pitanje.
- Peutz-Jeghersov sindrom: Brojni hamartomatozni polipi cijelog GI trakta; polipi su češći u tankom crijevu nego u kolonu; GI krvarenje je često; rizik za razvoj raka na GI i ne-GI mjestima. Ne savjetuje se profilaktični kirurški zahvat.
RAK KOLONA
Drugi najčešći rak unutarnjih organa u ljudi. Računa se da u SAD-u na njega otpada 10% smrtnih slučajeva izazvanih rakom; incidencija se dramatično povećava u dobi iznad 50 godina, gotovo jednako u muškaraca i žena. U 2015. godini 132.700 novih i 49.700 smrtnih slučajeva.
Etiologija i čimbenici rizika
Većina karcinoma kolona nastaje iz adenomatoznih polipa. Definiran je genetički slijed od polipa do displazije i karcinoma in situ do invazivnog karcinoma, uključujući: točkastu mutaciju K-ras protoonkogena, hipometilaciju DNK koja dovodi do pojačane ekspresije gena, gubitak alela na APC genu (tumorski supresor), gubitak alela na DCC genu (izbrisan kod raka kolona) na 18. kromosomu, te gubitak i mutacija p53 na 17. kromosomu. Nasljedni nepolipozni rak kolona nastaje zbog mutacije gena za popravak oštećenja/nepodudarnosti na DNK, mutacije hMSH2 gena na 2. kromosomu i hMLH1 gena na 3. kromosomu. Mutacije uzrokuju rak kolona i rak drugih sijela. Za postavljanje dijagnoze potrebno je da tri ili više rođaka imaju rak kolona, od kojih je jedan rođak u prvom koljenu; jedan ili više slučajeva dijagnosticiranih prije 50. godine života; zahvaćenost barem dvije generacije. Okolišni čimbenici također imaju ulogu; zračenje, pušenje. Prevalencija je veća u razvijenim zemljama, urbanim područjima, naprednim socioekonomskim skupinama. Rizik je povišen u bolesnika s hiperkolesterolemijom, koronarnom bolešću; povećan rizik uključuje prehranu siromašnu vlaknima, bogatu mastima životinjskog podrijetla premda izravan učinak prehrane nije dokazan. Rizik smanjuje dugotrajno nadomjesno uzimanje kalcija i vjerojatno, svakodnevno uzimanje ASK-a. Rizik je povećan u prvih rođaka oboljelih; u obiteljima s povećanom prevalencijom raka; u pacijentica s rakom dojke i ginekološkim rakom u anamnezi; kod sindroma obiteljske polipoze; kada ulcerozni kolitis ili Crohnov kolitis traju >10 godina; >15 godina ureterosigmoidostome. Tumori u bolesnika s jako pozitivnom obiteljskom anamnezom maligniteta često su lokalizirani u desnom kolonu i obično se javljaju prije 50. godine života; prevalencija je visoka u bolesnika sa Streptococcus bovis bakterijemijom.
Patologija
Gotovo su uvijek adenokarcinomi; u 75% slučajeva smješteni su distalno od lijenalne fleksure (osim uz slučaju popratne polipoze ili hereditarnih malignih sindroma); tumor može biti polipoidan, sesilan, gljivast ili konstriktivni; podtip i stupanj diferencijacije nije u korelaciji s tijekom bolesti. Stadij invazivnosti utvrđen pri kirurškom zahvatu (Dukesova klasifikacija) najbolji je samostalni prognostički pokazatelj (Sl. 71-1). Rektosigmiodni tumori mogu se rano širiti u pluća zbog sustavne paravertebralne venske drenaže ovog područja. Drugi loši prognostički pokazatelji: prijeoperativna vrijednost serumskog karcinoembrionalnog antigena (CEA) >5ng/ml (>5 µg/L), loša histološka diferencijacija, perforacija crijeva, prodor u venu, zahvaćanje susjednih organa, aneuploidija, specifične delecije na 5., 17. i 18. kromosomu i mutacija ras-protoonkogena. U 15% slučajeva popravak DNK je nepotpun.
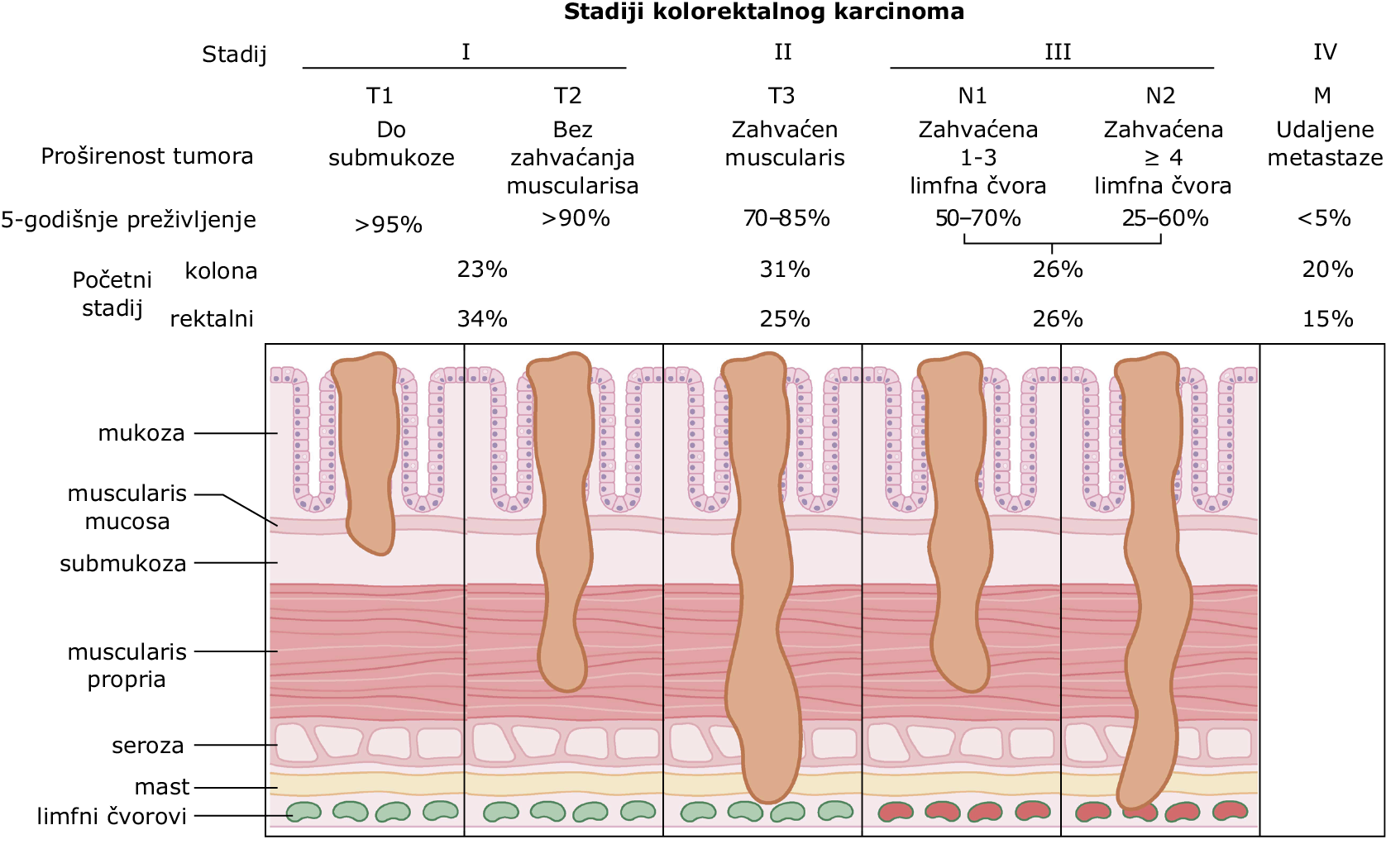
SLIKA 71-1 Određivanje stadija (stupnjevanje) i prognoza za bolesnike s rakom debelog crijeva.
Klinička slika
Ljevostrani rak kolona obično se očituje rektalnim krvarenjem, izmijenjenim crijevnim navikama (tankom stolicom, opstipacijom, povremenom dijarejom, tenezmima), bolovima u trbuhu ili leđima. Rak cekuma i uzlaznog kolona češće se očituje simptomima anemije, skrivenim krvarenjem u stolici ili mršavljenjem. Ostale komplikacije su: perforacija, fistula, volvulus, ingvinalna hernija. Laboratorijski nalazi: anemija u 50% desnostranih lezija.
Dijagnoza
Rana dijagnoza se postavlja probirom (screening) asimptomatskih osoba na okultno krvarenje u stolici (vidi ispod); >50% svih karcinoma kolona nalazi se unutar dosega 60-cm fleksibilnog sigmoidoskopa; zrak-kontrast barijska klizma otkrit će ~85% karcinoma kolona koji nisu unutar dosega sigmoidoskopa. Kolonoskopija je najosjetljivija i najspecifičnija pretraga, omogućuje biopsiju tumora i odstranjivanje sinkronih polipa (i na taj način prevenciju neoplastične konverzije), ali je skuplja. Radiološka ili virtualna kolonoskopija nije se pokazala boljom dijagnostičkom pretragom od kolonoskopije.
LIJEČENJE RAK KOLONA
Lokalna bolest: Kirurška resekcija segmenta kolona u kojem se tumor nalazi. Prijeoperativna obrada radi procjene prognoze i kirurškog pristupa uključuje kompletnu kolonoskopiju, RTG prsnog koša, biokemijske jetrene testove, razinu CEA u plazmi i po potrebi CT abdomena. U pojedinim je slučajevima moguća resekcija izoliranih jetrenih metastaza. Adjuvantna iradijacija zdjelice (sa ili bez konkomitantne kemoterapije 5-fluorouracilom) smanjuje postotak lokalnog recidiva karcinoma rektuma (bez jasnog učinka na preživljavanje). Radioterapija nije od koristi za tumore kolona. Prijeoperativna radioterapija može poboljšati resektabilnost i lokalnu kontrolu u bolesnika s karcinomom rektuma. Totalna mezorektalna ekscizija je učinkovitija od standardne anteroposteriorne resekcije kod karcinoma rektuma. Adjuvantna kemoterapija (5-FU/leukovorin + oksaliplatina ili FOLFOX + bevacizumab, ili 5FU/leukovorin plus irinotekan, ili FOLFIRI) smanjuje postotak recidiva i poboljšava preživljavanje kod stadija C (III), vjerojatno i kod stadija B (II). Periodično određivanje razine serumskog CEA služi za praćenje terapijskog odgovora i otkrivanje recidiva. Praćenje nakon kurativne resekcije: Svake godine jetreni testovi, KKS, radiološka ili kolonoskopska kontrola nakon 1 godine—ukoliko je nalaz normalan, ponavljati svake 3 godine uz rutinsko pretraživanje u međuvremenu (vidi ispod); ukoliko se otkriju polipi, ponavljati 1 godinu nakon resekcije. Uznapredovali tumor (lokalno neresektabilni ili metastatski): sistemska kemoterapija (5 FU/leukovorin + oksaliplatina + bevacizumab), irinotekan se obično koristi kao II. linija liječenja; anti-EGFR protutijela (cetuximab, panitumumab) za koja se čini da poboljšavaju učinak kemoterapije, ali nisu djelotvorna u tumora s RAS mutacijom; nadalje intraarterijska kemoterapija [floksuridin (FUDR)] i/ili radioterapija mogu ublažiti simptome jetrenih metastaza. Solitarne jetrene metastaze se mogu resecirati parcijalnom hepatektomijom sa 25% 5-godišnjim preživljavanjem.
Prevencija
Rano otkrivanje karcinoma kolona može se pospješiti rutinskim pretraživanjem stolice na okultno krvarenje (Hemoccult II, ColonCare, Hemosure, itd.). Međutim, osjetljivost iznosi ~50% za karcinom; specifičnost za tumor ili polip iznosi ~25–40%. Noviji testovi će uključivati detekciju krvi i mutacije gena, s većom osjetljivošću i specifičnošću Lažno pozitivni: konzumiranje crvenog mesa, željeza, ASK, krvarenje iz gornjeg GI trakta. Lažno negativni: uzimanje C vitamina, povremeno krvarenje. Godišnji digitorektalni pregled i pregled stolice na skriveno krvarenje preporučuje se bolesnicima iznad 40. godine života, pretraživanje fleksibilnom sigmoidoskopijom svake 3 godine nakon 50. godine života, ranije u bolesnika s povećanim rizikom (vidi ispod). Pažljiva evaluacija svih bolesnika s pozitivnim testom na okultno krvarenje (fleksibilna sigmoidoskopija i zrak-kontrast barijska klizma ili samo kolonoskopija) otkriva polipe u 20–40% slučajeva i karcinom u ~5%. Probir asimptomatskih osoba omogućuje rano otkrivanje raka kolona (npr. raniji Dukesov stadij) pa je postotak operabilnosti veći. Smanjena ukupna smrtnost od karcinoma kolona uočava se tek nakon 13 godina praćenja. Intenzivnije praćenje rođaka u prvom koljenu oboljelih od karcinoma kolona obično uključuje probir barijskom klizmom zrak-kontrast ili kolonoskopijom nakon dobi od 40 godina. Pokazalo se da NSAR i inhibitori ciklooksigenaze 2 sprječavaju razvoj polipa i potiču regresiju kod visoko rizičnih skupina, ali se za sada ne preporučuju pacijentima s prosječnim rizikom.
RAK ANUSA
Na njega otpada 1–2% tumora debelog crijeva, 7210 novih i 1100 smrtnih slučajeva u 2015. godini. Povezuje se s kroničnom iritacijom, npr. condyloma accuminata, perianalne fisure/fistule, kronični hemeroidi, leukoplakija, trauma nastala analnim snošajem. Etiologija je HPV. Obično češće pogađa žene nego muškarce. Homoseksualci imaju veći rizik. Očituje se krvarenjem, bolovima, perianalnom tvorbom. Radioterapija i kemoterapija (5-FU i mitomicin) dovode do potpunog terapijskog odgovora u 80% slučajeva kad je primarna lezija <3 cm. Abdominoperinealna resekcija s trajnom kolostomom rezervirana je za one s velikom lezijom i za one s recidivom bolesti nakon kemoradioterapije.
BENIGNI TUMORI JETRE
Hepatocelularni adenomi najčešće se javljaju u žena u 3. i 4. desetljeću koje uzimaju oralne kontraceptive. Većina ih se pronađe slučajno, ali mogu uzrokovati i bol. Intratumorsko krvarenje može dovesti do cirkulacijskog kolapsa. Rizik od maligne pretvorbe iznosi 10%. Žene s tim adenomima trebaju prestati uzimati oralne kontraceptive. Veliki tumori blizu površine jetre mogu se odstraniti kirurški. Fokalna nodularna hiperplazija je također češća u žena, ali izgleda da nije uzrokovana oralnim kontraceptivima. Lezije su na angiografiji vaskularne i imaju pregrade pa su obično asimptomatske.
HEPATOCELULARNI KARCINOM
Oko 35.660 slučajeva u SAD-u 2015. godine, 24.550 smrtnih, ali diljem svijeta to može biti najčešći tumor. Omjer, muški spol:ženski spol = 4:1. Tumor se obično razvija u cirotičnoj jetri osoba u 5. ili 6. desetljeću života. Visoka incidencija u Aziji i Africi rezultat je uzročne povezanosti ovog karcinoma i hepatitisa B i C. Cjepivo protiv B hepatitisa i liječenje hepatitisa C bi trebalo smanjiti incidenciju. Izloženost aflatoksinu doprinosi etiologiji i ostavlja molekularni potpis, mutaciju na kodonu 249 gena za p53.
Prezentacija
Pacijent s poznatom bolesti jetre može imati suspektan pozitivni nalaz ultrazvuka ili viši alfa-fetoprotein (AFP) ili des-gama-karboksi protrombin (DKP) zbog smanjenog vitamina K; abnormalne jetrene enzime, kaheksiju, abdominalnu bol, vrućicu.
Fizikalni nalaz
Žutica, astenija, svrbež, tremor, dezorijentacija, hepatomegalija, splenomegalija, ascites, periferni edemi i slično.
LIJEČENJE HEPATOCELULARNI KARCINOM
Liječi se kirurškom resekcijom ili transplantacijom jetre, ali rijetko uspješno. Radiofrekventna ablacija, transarterijska kemoembolizacija (TACE) i itrij mogu dovesti do regresije manjih tumora. Sorafenib daje nepotpune rezultate u trajanju od par mjeseci.
Probir i prevencija
Probir rizičnih populacija je dao proturječne rezultate. Interferon α može spriječiti rak jetre u osoba s kroničnim aktivnim hepatitisom C i moguće u onih s hepatitisom B. Prevencija hepatitisa B cjepivom. Kombinirana terapija inhibitorom virusne proteaze (npr. ledipasvir), te inhibitorom virusne polimeraze (npr. sofusbuvir) u trajanju od 12–24 tjedana izliječi većinu pacijenata s hepatitisom C.
RAK GUŠTERAČE
Oko 48.960 novih i 40.270 smrtnih slučajeva u SAD-u 2015. godine. Incidencija se nešto smanjuje, ali su gotovo svi dijagnosticirani slučajevi fatalni. Tumori su duktalni adenokarcinomi pa se obično ne mogu otkriti dok se bolest ne proširi. Oko 70% tumora smješteno je u glavi gušterače, 20% u tijelu i 10% u repu. Mutacije K-ras nađene su u 85% tumora, a može biti upleten i p16 inhibitor kinaze ovisan o ciklinu na 9. kromosomu. Dugotrajni dijabetes, kronični pankreatitis i pušenje povećavaju rizik, a pijenje kave, alkoholizam i kolelitijaza ne. Bolesnici se tuže na bol i gubitak tjelesne težine, a bol često popušta naginjanjem prema naprijed. Žutica je česta komplikacija kod tumora glave zbog bilijarne opstrukcije. Kurativna kirurška resekcija je moguća u oko 10% slučajeva. Adjuvantna kemoterapija može koristiti nekim bolesnicima nakon resekcije. Gemcitabin plus erlotinib ili capecitabine može ublažiti simptome kod uznapredovale bolesti. Pacijenti u dobrom fizičkom stanju bi mogli imati koristi od politerapije, FOLFIRINOX, što uključuje 5FU, irinotekan i oksaliplatinu.
ENDOKRINI TUMORI PROBAVNOG TRAKTA I GUŠTERAČE
KARCINOIDNI TUMOR
Na karcinoidni tumor otpada 75% svih GI endokrinih tumora. Incidencija iznosi oko 15 slučajeva na milijun, od kojih, 90% potječe iz Kulchitskyjevih (enterokromafinih) stanica GI trakta, najčešće iz apendiksa, ileuma i rektuma. Karcinoidni tumori tankog crijeva i bronha imaju maligniji tijek od tumora drugih sijela. Oko 5% bolesnika s karcinoidnim tumorima ima simptome karcinoidnog sindroma, klasični trijas koji čine crvenilo lica, proljev i bolest srčanih zalistaka. Za tumore koji potječu iz GI trakta, simptomi podrazumijevaju metastaze u jetru.
Dijagnoza se može postaviti otkrivanjem sijela tumora ili dokazivanjem produkta metabolizma serotonina, 5-hidroksiindoloctene kiseline (5-HIAA) u urinu, >15 mg/dan. Scintigrafija oktreotidom omogućuje otkrivanje sijela primarnog i metastatskog tumora u oko 2/3 slučajeva.
LIJEČENJE KARCINOIDNI TUMOR
Kirurška resekcija kad god je moguće. Simptomi se mogu kontrolirati blokatorima histamina, blokatorima serotoninskih receptora i oktreotidom, 150–1500 mg/dan u tri doze. Embolizacija hepatalne arterije i kemoterapija (5-FU plus streptozocin ili doksorubicin) primjenjuju se za metastatsku bolest. IFN-α, 3–10 milijuna jedinica SC tri puta tjedno može olakšati simptome. Prognoza varira od 95%-tnog petogodišnjeg preživljavanja za lokaliziranu bolest do 20%-tnog petogodišnjeg preživljavanja za one s jetrenim metastazama. Srednje vrijeme preživljavanja za bolesnike s karcinoidnim sindromom iznosi 2,5 godine od prvog napada navale crvenila.
TUMORI STANICA OTOČIĆA GUŠTERAČE
Gastrinom, inzulinom, VIP-om, glukagonom i somatostatinom čine glavninu tumora stanica otočića gušterače. Njihove karakteristike prikazuje Tbl. 71-3. Tumori su imenovani prema glavnom hormonu kojeg proizvode. Obično su spororastući i uzrokuju simptome vezane za stvaranje hormona. Zollinger-Ellisonov sindrom uključuje gastrinome i peptičku ulkusnu bolest. Gastrinomi su rijetki (4 slučaja na 10 milijuna ljudi); u 25–50% slučajeva tumor je sastavni dio MEN I sindroma.
TABLICA 71-3 GASTROINTESTINALNI ENDOKRINI TUMORI
|
|
Sindrom
|
Tip stanica
|
Klinička obilježja
|
Postotak malignih
|
Glavni produkti
|
|
Karcionoidni sindrom
|
Enterokromafine i stanice nalik enterokromafinim
|
Crvenilo lica, zvižduci (bronhopstrukcija), dijareja, hipotenzija
|
~100
|
Serotonin, histamin, ostali peptidi
|
|
Zollinger-Ellisonov gastrinom
|
Ne-β stanice otočića gušterače, duodenalne G stanice
|
Peptični ulkusi, dijareja
|
~70
|
Gastrin
|
|
Inzulinom
|
β stanice Langerhansovih otočića
|
Hipoglikemija
|
~10
|
Inzulin
|
|
VIPom (Verner- Morrison, WDHA)
|
D1 stanice Langerhansovih otočića
|
Dijareja, hipokalijemija, hipokloridija
|
~60
|
Vazoaktivni intenstinalni peptid
|
|
Glukagonom
|
α stanice Langerhansovih otočića
|
Blagi dijabetes, erythema necrolytica migrans, glositis
|
>75
|
Glukagon
|
|
Somatostatinom
|
D stanice otočića
|
Dijatebes, dijareja, steatoreja, žučni kamenci
|
~70
|
Somatostatin
|
|
Kratice: WDHA = vodenasti proljev, hipokalijemija, aklorhidrija (engl. watery diarrhea, hypokalemia, achlorhydria).
|
Inzulinom se može očitovati Whippleovim trijasom: hipoglikemija natašte, simptomi hipoglikemije, olakšanje nakon intravenskog davanja glukoze. Normalne ili povišene vrijednosti inzulina u serumu uz hipoglikemiju natašte omogućuju postavljanje dijagnoze. Inzulinomi također mogu biti udruženi s MEN I.
Verner i Morrison su opisali sindrom vodenih proljeva, hipokalijemije, aklorhidrije i zatajenja bubrega povezan s tumorima stanica otočića gušterače koji proizvode vazoaktivni intestinalni polipeptid (VIP). VIP-omi su rijetki (1 slučaj na 10 milijuna), ali često narastu do ogromnih veličina prije nego izazovu simptome.
Glukagonom je povezan s dijabetesom i nekrolitičkim migrirajućim eritemom za koji je karakterističan crveni, uzdignuti, ljuskasti osip obično lokaliziran na licu, trbuhu, perineumu i distalnim ekstremitetima. Razina glukagona >1000 ng/L koju nije moguće suprimirati glukozom potvrđuje dijagnozu.
Klasični trijas somatostatinoma je diabetes mellitus, steatoreja i kolelitijaza.
Provokacijski testovi mogu olakšati dijagnozu funkcionalnih endokrinih tumora: tolbutamid pojačava sekreciju somatostatina kod somatostatinoma, pentagastrin pojačava sekreciju kalcitonina iz medularnih tumora štitnjače (C stanice); sekretin pojačava sekreciju gastrina iz gastrinoma. Ukoliko slikovnim pretragama ne uspijemo otkriti tumorsku masu, angiografija ili određivanje hormona selektivnim skupljanjem venske krvi može otkriti tumorsko sijelo. CT ili MR može naći metastaze u čvorove i jetru.
LIJEČENJE TUMORI STANICA OTOČIĆA GUŠTERAČE
Ukoliko je moguće, tumor treba kirurški odstraniti. Everolimus (10 mg per os 1×/dan) ili sunitinib (37,5 per os, također 1×/dan) mogu značajno odgoditi progresiju bolesti i produžiti preživljenje u bolesnika koji imaju metastatsku bolest. Oktreotid inhibira sekreciju hormona u većini slučajeva. IFN-α može ublažiti simptome. Polikemoterapija (streptozocin plus doksorubicin) može dovesti do terapijskog odgovora u 60–90% slučajeva. Embolizacija jetrenih presadnica ima palijativni učinak.
Opširnije vidi u Mayer RJ: Rak gornjeg probavnog trakta, Pogl. 109, str. 532; Mayer RJ; Rak donjeg probavnog trakta, Pogl. 110, str. 537; Carr BI: Tumori jetre i bilijarnog stabla, Pogl. 111. str. 544; Smyth E, Cunningham D: Pankreatični rak, Pogl. 112. str. 554; i Jensen RT: Endokrini tumori gastrointestinalnog trakta i pankreasa, Pogl. 113, str. 557, u HPIM-19.